கீற்றில் தேட...
அறிவியல் ஆயிரம்
- விவரங்கள்
- இராசேந்திர சோழன்
- பிரிவு: தொழில்நுட்பம்
அணுக்கருவுக்குள் நுழையும் போதுதான் அணு ஆற்றல் பற்றிப் புரிந்து கொள்ள முடியும் என்றாலும் அணு ஆற்றல் பற்றி அறிந்து கொள்ளுமுன் பொதுவாக ஆற்றல் என்றால் என்ன என்று பார்த்துக் கொண்டு மேலே செல்வோம்.
“ENERGY” என்கிற ஆங்கிலச் சொல்லே தமிழில் “ஆற்றல்” அல்லது “சக்தி” என்று அழைக்கப்படுகிறது. இந்த ஆற்றல் அல்லது சக்தி என்பது என்ன?
இந்த ஆற்றல் என்பது நேரடியாகக் கண்ணால் காண முடியாதது. அதற்கு நிறம் கிடையாது. மணம் கிடையாது. ருசி கிடையாது. இதரப் பொருள்களை நேரடியாகக் கையால் தொட்டு உணர்வது போல ஆற்றலைத் தொட்டு உணரவோ, நமது புலன்களால் நேரடியாக அறியவோ முடியாது. பிறகு, நாம் ஆற்றலை எப்படித்தான் காண்கிறோம்? எப்படித்தான் அறிகிறோம்? ஆற்றலை நாம் அது இயங்கும் பொருள்களின் மூலமாக மட்டும் பார்க்கிறோம். அந்தப் பொருள்களின் வாயிலாகவே அறிகிறோம். எப்படி?
கார் ஓடுகிறது. இரயில் ஓடுகிறது. ஆகாய விமானம் பறக்கிறது. நீர் இறைக்கும் என்ஜின் அல்லது மின்சார மோட்டார் இயங்குகிறது. மின்விளக்கு எரிகிறது. மின்விசிறி சுழல்கிறது... இவையெல்லாம் எப்படி இயங்குகின்றன? இவையெல்லாம் அது அதற்கும் தேவைப்படும் பல்வேறு ஆற்றல்களை, அந்த ஆற்றல்களைத் தரும் பல்வேறு விதப் பொருள்களைக் கொண்டே இயங்குகின்றன. இப்பொருள்கள் பெட்ரோல், டீசல், நீராவி, மின்சாரம் என இப்படிப் பலதரப்பட்டு இருக்கின்றன.
இது பிற பொருள்கள் இயங்க என்று மட்டும் இல்லை. நாம் நடக்க, ஓட, உட்கார, எழுந்திருக்க, பல்வேறு வேலை களைச் செய்ய நமக்கும் ஆற்றல் தேவைப்படுகிறது. இந்த ஆற்றல் நமக்கு எங்கிருந்து கிடைக்கிறது? நாம் உண்ணும் உணவிலிருந்து, உட்கொள்ளும் சுவாசத்திலிருந்து கிடைக் கிறது இல்லையா? சரி. ஆகவே பொதுவில் மனித இயக்கத் திற்கும் பிற பொருள்கள் இயக்கத்திற்கும் ஆற்றல் தேவைப் படுகிறது. இந்த ஆற்றல் பலவகைப்பட்டதாய் இருக்கிறது.
ஆற்றல் இப்படிப் பலவகைப்பட்டதாய் இருந்தாலும் மொத்தத்தில் பொதுவாய் இந்த ஆற்றல்களை எட்டு வகையாகப் பிரிக்கலாம். அவையாவன :
1. வேதி ஆற்றல்
2. வெப்ப ஆற்றல்
3. எந்திர ஆற்றல்
4. மின் ஆற்றல்
5. ஒளி ஆற்றல்
6. ஒலி ஆற்றல்
7. மின்காந்த ஆற்றல்
8. அணு ஆற்றல்
இவை வெவ்வேறு வகையில் பெறப்படுவதாலேயே இவை வெவ்வேறு பெயரால் அழைக்கப்படுகின்றன.
காட்டாக, பெட்ரோல், டீசல், நாம் உண்ணும் உணவு, காய்கறிகள், பழங்கள், மாமிசம் இவற்றிலிருந்து பெறப்படும் ஆற்றல் வேதி ஆற்றல்.
சூரியனிடமிருந்து நேரடியாக நாம் பெறுவது, நிலக்கரி வெப்பத்தைப் பயன் படுத்தி நீராவி மூலம் இரயில் ஓட்டுவது, கப்பல் ஓட்டுவது எல்லாம் வெப்ப ஆற்றல். பார்க்கப்போனால் நம் உடம்பில் நிகழும் இரத்த ஓட்டம் உட்பட யாவும் நமது இதயத்தின் எந்திர இயக்கம் காரணமாகப் பெறப்படுகிற ஆற்றல்தான்.
இதேபோலவே ஒலி,ஒளி,மின்சாரம், காந்தம், மின் காந்தம் அணு இவைகளிலிருந்து பெறப்படும் ஆற்றல்கள் எல்லாம் அந்தந்த வகை ஆற்றல்களாகப் பெயரிட்டு அழைக்கப்படுகின்றன.
இங்கே ஒரு முக்கிய விஷயம். மேலே இப்படி ஆற்றல்களை வகைப்படுத்திச் சொல்வதால், இவ்வாற்றல்கள் எல்லாம் முற்றாகத் தனித்தனியானவை என்றோ, அல்லது இவை ஒன்றுக்கொன்று சம்பந்தமே இல்லாதவை என்றோ யாரும் தவறாகக் கருதிவிடக் கூடாது. காரணம் இவையெல்லாம் ஒன்றுக்கொன்று சம்பந்தமுடையவை. ஒன்றோடொன்று தொடர்புடையவை. ஒன்று மற்றொன்றாக மாறத்தக்கவை. இப்படி மாறும் சாத்தியமுள்ளதாய் இருப்பதனாலேயே இவை நமக்குப் பயன் தருவதாயும் இருக்கின்றன. நம்மால் பயன்படுத்தவும் முடிகிறது. எப்படி?
நீரைக்கொண்டு, டர்பைனை இயக்கி அதாவது எந்திர ஆற்றலை உருவாக்கி, அந்த எந்திர ஆற்றலில் இருந்து மின் ஆற்றலைப் பெறுகிறோம். அந்த மின் ஆற்றல் ஒளியாற்றலாக, வெப்ப ஆற்றலாக மாறி, மின் விளக்கு எரிகிறது. மின் இஸ்திரிப் பெட்டி சூடாகிறது. எந்திர ஆற்றலாக மாறி மின்விசிறி சுழல்கிறது. மின்சார மோட்டார், மாவு அரைக்கும் யந்திரங்கள் இயங்குகின்றன.
அதேபோல டீசலைப் பயன்படுத்தி, அதாவது வேதியியல் வகை ஆற்றலைப் பயன்படுத்தி, ஜெனரேட்டரை இயங்கச் செய்கிறோம். அதாவது எந்திர ஆற்றலைப் பெறுகிறோம். இந்த ஜெனரேட்டரை இயங்கச் செய்து மின்ஆற்றலைப் பெறுகிறோம்.
சூரியனிடமிருந்து வெப்ப ஆற்றலைப் பெற்று மரம் செடி, கொடி தாவரங்கள் வளர்கின்றன. அவற்றின் காய்கறிகள் பழங்களைத் தின்று வேதியியல் ஆற்றலாக மாற்றி நாம் நம் இயக்கத்துக்கான யந்திர ஆற்றலைப் பெறுகிறோம்.
அதேபோலப் பல ஆயிரக்கணக்கான ஆண்டுகளுக்கு முன் வாழ்ந்து மடிந்த தாவரங்களும், விலங்குகளும் பூமிக்கடியில் மக்கி நிலக்கரியாகவும், டீசல் பெட்ரோல் ஆகவும் நமக்குக் கிடைக்கிறது. இப்படியே பலவும்.
இதிலிருந்து நமக்கு என்ன தெரிகிறது...?
பேரண்டத்தில் நிலவும் ஆற்றல் பலவகைப்பட்டதாய் இருக்கிறது. இந்த ஆற்றல்கள் ஒன்று மற்றொன்றாக மாறத் தக்கவை. இப்படி மாறத்தக்க ஆற்றல்களாக இவை இருப்பதனாலேயே இவை நமக்குப் பயன்படும் ஆற்றல்களாக, அதாவது நம்மால் பயன்படுத்த முடிந்த ஆற்றல்களாகவும் இருக்கின்றன. இல்லையா? சரி. இது அப்படியே இருக்கட்டும்.
ஆற்றல் மாற்றமும் பலனும்
இயற்கையின் எல்லா இயக்கத்துக்கும் விதிமுறைகள் இருப்பது போலவே ஆற்றலுக்கும் விதிகள் உண்டு. இந்த விதிகளில் ஒன்றை ஏற்கெனவே பார்த்தோம். அதாவது ஒரு ஆற்றல் இன்னொன்றாக மாறத்தக்கது. மாற்ற சாத்தியமுடையது என்பதே அது.
சரி, ஆற்றல் பற்றிய இன்னொரு விதி ஆற்றலை ஆக்கவும் முடியாது, அழிக்கவும் முடியாது என்பதே.
எப்படி எந்தப் பொருளையும் ஆக்கவும் முடியாது, அழிக்கவும் முடியாதோ, அதாவது இதை மேலோட்டமாகப் புரிந்து கொண்டு எதிர் கேள்வி போடாமல், இந்தக் கூற்றின் அறிவியல் அர்த்தத்தில், எந்த ஒரு பொருளையும் ஏதாவது ஒரு பொருளிலிருந்து தான் உருவாக்க முடியும், அதேபோல எந்த ஒரு பொருளை அழிக்க நினைத்தாலும் அது இன்னொரு பொருளாகத்தான் மாறுமே தவிர அது அழியாது என்பதை எப்படிப் புரிந்து கொள்கிறோமோஅதைப்போல, காட்டாக, இயற்கையில் காணும் பொருள்கள் தவிர மனிதன் புதிது புதிதாக எவ்வளவோ பொருள்களைச் செய்கிறான் என்றாலும் இப்படிச் செய்யும் எல்லா பொருளும் இயற்கையில் காணும் ஏதாவது ஒரு அல்லது பல பொருள்களிலிருந்தே உருவாக்கப்படுகின்றன என்பதை எப்படி அறிகிறோமோ அதேபோல எந்த ஆற்றலையும் அழிக்க நினைத்தால் அது இன்னொரு ஆற்றலாகத்தான் மாறுமே தவிர அந்த ஆற்றல் அழியாது என்பதையும் நாம் புரிந்துகொள்ள வேண்டும்.
எப்படி? விறகு இருக்கிறது. அது ஒரு பொருள். எரிந்து மறைந்து விடவில்லையா, பெட்ரோல் இருக்கிறது. அது ஒரு பொருள். அது எரிந்தோ அல்லது காற்றில் ஆவியாகியோ மறைந்து விடவில்லையா என்று சிலர் நினைக்கலாம். ஆனால், அது உண்மையில்லை. மறைவது பொருட்களின் வடிவம் தானேயொழிய முற்றாக அதில் அடங்கியுள்ள பொருட்கள் அல்ல. அவை அழியவும் முடியாது. காரணம் ஏற்கெனவே அணு, தனிமம், மூலக்கூறு பற்றியெல்லாம் படித்தோமில்லையா... அதைச் சற்று நினைவு கொள்வோம். அப்படி நினைவு கொள்ள, விறகு எப்படிப்பட்ட மூலக் கூறுகளால், தனிமங்களால் ஆக்கப்பட்டதோ, அவை விறகு எரியும் போதும் அழிந்துபடாமல் வேதிவினை புரிந்து வேறொரு பொருளின் மூலக்கூறுகளாக, தனிமங்களாக மாறிவிடுகின்றன. அதாவது விறகு எப்படிப் பட்ட பொருட்களால் ஆக்கப்பட்டதோ, அவற்றின் மூலக் கூறுகள் அல்லது தனிமத் துகள்கள் அழியாமல் அவை அப்படியே வேறொரு பொருளின் மூலக் கூறுகளாக தமினிமங்களாகாக மாறி விடுகின்றன. அதாவது விறகு என்கிற பொருள் மறைந்து வேறு பல பொருள்கள் வடிவில் அவை நிலவுகின்றன.
இப்படியே பெட்ரோலும் மற்ற எரிபொருட்களும் எல்லாமும். இப்போது பொருள் அழிவதில்லை என்பதை ஓரளவு புரிந்து கொள்ள முடிகிறது இல்லையா..? சரி. ஆற்றல் அழிவதில்லை என்பதை எப்படிப் புரிந்து கொள்வது?
காட்டாக, அருவியிலிருந்து மின்சாரம் எடுக்கிறோம். அருவியில் கொட்டும் நீர் அதன் வேகம் என்பது ஒரு ஆற்றல், மின்சாரம் என்பதும் ஒரு ஆற்றல். ஆகவே இங்கு நீரின் இயக்க ஆற்றல் மின் ஆற்றலாக மாறுகிறது. அந்த ஆற்றலிலிருந்து பல்பு எரிகிறது. பல்பு எரிவதன் மூலம் மின் ஆற்றல், வெப்ப, ஒளி ஆற்றலாக மாறி வளிமண்டலத்தில் கரைந்து விடுகிறது. மின்விசிறியாகச் சுழன்று இதுவும் வளிமண்டலத்தை வெப்பமூட்டி விசும்பில் கரைந்து விடுகிறது. அதாவது மின் விளக்கு, மின் விசிறி வெளிப்படுத்தும் ஆற்றல் நம்மைச் சுற்றியுள்ள வளி மண்டலத்தை வெப்பமூட்டும் ஆற்றலாக மாறிவிடுகிறது.
இதேபோலப் பெட்ரோல் திறந்து வைத்திருந்தால் அது ஆவியாகி வளி மண்டலத்தில் கரைந்து வளிமண்டலத்தை வெப்பப்படுத்துகிறது. அதாவது வளிமண்டலத்தில் இருந்து வெப்பத்தை எடுத்துக் கொண்டுஆவியாகி அதன்மூலம் மீண்டும் வளிமண்டலத்தை வெப்பமூட்டுகிறது. மோட்டார், கார் யந்திரங்களை இயங்கச் செய்து ஓட்டினாலும், அது காற்றைக் கிழித்துக் கொண்டு ஓடி வளிமண்டலத்தை வெப்பமூட்டி அதில் கரைந்து விடுகிறது. அதாவது வளிமண்டலத்தில் கரைந்து விடுகிறது என்றுதான் சொல்கிறோமே தவிர மறைந்து விடுவதில்லை. மறைந்து காணாமல் போய்விடுவதில்லை. மாறாக, அது வேறொரு வடிவத்தில் வேறொரு ஆற்றலாக விசும்பில் கலந்திருக்கிறது என்பதே இதன் பொருள்.
இதனால்தான் விஞ்ஞானிகள் ஆற்றலை அழிக்கவோ ஆக்கவோ முடியாது என்றும், ஆகவே பிரபஞ்சத்தில் நிலவும் மொத்த ஆற்றல் எப்போதும் மாறாது ஒரே நிலையில் இருக்கிறது என்றும், ஆனால் அது தொடர்ச்சியாக ஒன்று மற்றொன்றாக மாறிக் கொண்டிருப்பதின் இயக்கத்தில் இருக்கிறது என்றும், இப்படி இயக்கத்தில் இருந்தாலும் இந்த இயக்கத்தின் மூலம் இப்பேரண்டத்தில் உள்ள மொத்த ஆற்றலின் அளவு கூடா மலும் அதாவது கூடுதலாக ஆக்கப்படாமலும், அதே சமயம் குறையாமலும் அதாவது கொஞ்சமேனும் அழிக்கப்படாமலும் ஒரே நிலையில் இருக்கிறது என்றும் கூறுகின்றார்கள்.
இதில், நமக்குக் கிடைக்கும் ஆற்றல்கள் பெருமளவும் அனைத்தும் பிரதானமாக வெப்ப ஆற்றல்கள் தொடங்கி, எந்திர ஆற்றல்களாக மாற்றப்பட்டு, நமக்குப் பயன் தந்து, மீண்டும் வெப்ப ஆற்றல்களாக மாறி, வளிமண்டலத்தில் கரைந்து, வளியை வெப்பப்படுத்துவதாகவே முடிவதைக் காணலாம்.
எல்லா எந்திர ஓட்டங்களிலிருந்தும், மனித உழைப்பின் எல்லா செயல்பாடுகள்வரையும் யோசிக்க இது புரியும். அதனால் தான் இந்த ஆற்றல் அதன் வடிவத்தில், பண்பில் மாற்றம் கொள்ளத்தக்கதாக இருந்தாலும் அளவில் எப்போதும் மாறாது ஒரே நிலையில் இருந்து வருகிறது.
அதோடு இந்த ஆற்றல் பற்றி இன்னொன்று. எந்த ஆற்றலையும் நம் வாழ்க்கைப் பயன் கருதியே அதை வேறொரு ஆற்றலாக மாற்றுகிறோம். என்றாலும் இந்தப் பயன்பாடு என்பது ஒரு ஆற்றல் இன்னொரு ஆற்றலாக மாறும் நிலையில் ஏற்படும் ஒரு இடைநிகழ்வு அல்லது புறநிகழ்வே தவிர, இந்தப் பயன்பாடே ஆற்றலின் முழுமையான வெளிப்பாடு அல்ல என்பதை நாம் புரிந்துகொள்ள வேண்டும். எப்படி?
பேனாவால் எழுதுகிறோம். எழுவது பயன்பாடு. ஆனால் எழுதுவதால் நிப்பு தேய்கிறது. நிப்பு தேய்வது ஆற்றல் மாற்றம். இடையில் இது எழுதியிருப்பது பயன்பாடு. அதாவது நிப்பு தேய்கையில் ஏற்பட்ட உடன் நிகழ்வு.
இதில் எழுதுவதற்கு என்றுதான் பேனா பிடிக்கிறோமே தவிர நிப்பைத் தேய்ப்பதற்காக அல்ல. ஆனாலும் நிப்பு தேய்வதைத் தவிர்க்க முடியாது. நிப்பு தேயாமல் எழுதவும் முடியாது. நிப்பைத் தேய்ப்பதும் நம் குறிக்கோள் அல்ல. அப்படியானால் நாம் எதையும் எழுதாமலேயேகூட நிப்பைத் தேய்க்கலாம் என்றாலும், நிப்பு தேய்வதைத் தவிர்த்து, அதாவது தேய்வதால் ஏற்படும் உராய்வு விசையைத் தவிர்த்து நம்மால் எழுத முடியாது.
பெட்ரோலை நிரப்பிக் கார் ஓட்டுகிறோம். கார் ஓடுகிறது, டயர் சுற்றுகிறது, சூடாகிறது, தேய்கிறது, கார் வளி மண்டலத்தைக் கிழித்துக் கொண்டு ஓடுவதால் கார் ஓடும் ஆற்றலுக்கேற்ப வளிமண்டலத்தைச் சூடாக்குகிறது. பெட்ரோலின் வேதியியல் ஆற்றலை யந்திர ஆற்றலாக மாற்றிக் காரை ஓட்டி கரியமில வாயுவை வெளி விட்டு நம்மை யறியாமலேயே வெப்ப ஆற்றலை உண்டு பண்ணி விசும்பில் கரைக்கிறோம்.
இதில் டயரைத் தேய்க்க வேண்டுமென்பதோ கரியமில வாயுவை வெளிவிட்டு வளிமண்டலத்தை வெப்பமுட்ட வேண்டு மென்பதோ நம் நோக்கம் அல்ல. அந்த நோக்கத்துக்கு நாம் கார் ஓட்டவும் இல்லை. நம்முடைய நோக்கம் ஓர் இடத்திலிருந்து இன்னோர் இடத்திற்குப் போக வேண்டுமென்பதே. ஆனால் மேற்கண்ட இரு நிகழ்வுகளையும் தவிர்த்து நம்மால் கார் ஓட்ட முடியுமா, நிச்சயம் முடியாது. இப்படி அன்றாடம் நாம் செய்யும் ஒவ்வொரு செயலையும் சிந்திக்க பலது புரியும்.
இதேபோலவே நாம் உண்கிறோம். வேலை செய்கிறோம். சக்தியை வெளிப்படுத்துகிறோம். வேலை செய்வதன் மூலமோ அல்லது உடற்பயிற்சி செய்வதன் மூலமோ சக்தி வெளிப் படுகிறது. இதுவும் விசும்பில் கலக்கிறது. ஆனால் இதற் கிடையில் எவ்வளவோ பயன்படு பொருள்களைச் செய்கிறோம்.
இன்னும் தொழிற்சாலைப் புகைபோக்கிகள் கக்கும் கரும்புகைகள், வெளிப்படுத்தும் கழிவுநீர்கள், இதுவும் ஆற்றலின் ஒரு வடிவம்தான். ஆனால் இந்தப் புகையையும், கழிவுநீரையும் வெளிப்படுத்த வேண்டும் என்பதல்ல தொழிற் சாலையை நிர்மாணிப்பதன் நோக்கம், அதில் குறிப்பிட்ட சில பொருள்களை உற்பத்தி செய்ய வேண்டும் என்பதே. ஆனால் இக் கரும் புகையையும், கழிவுநீரையும் வெளிப்படுத்தாமல் அத்தொழிற் சாலை இயங்க முடியாது, பொருள்களை உற்பத்தி செய்யவும் முடியாது இல்லையா? இப்படியே பலதும்.
சரி. இதிலிருந்து நாம் அறிவது என்ன? இயற்கையாகவோ, அல்லது மனித முயற்சியில் செயற்கையாகவோ ஆற்றல் என்பது எப்போதும் வெவ்வேறு வடிவங்களுக்கு மாறிக்கொண்டேயிருக்கிறது என்பதுதானே?
இப்படி மாறிக் கொண்டிருக்கும் ஆற்றலில், ஒன்று மற்றொன்றாக மாறும் நிலையில் ஏற்படும் ஓர் உடன் நிகழ்வு அல்லது புற நிகழ்வே நம் பயன்பாடு என்பது. எனவே இந்தப் பயன்பாடு என்பது ஆற்றல் மாற்றம் இல்லாமல் சாத்தியப்பட முடியாது என்பதுதானே? சரி இருக்கட்டும்.
ஆக, ஆற்றல் மாற்றத்தக்கது. எனில். அது அழியாதது. அதேவேளை அது புற விளைவுகளை ஏற்படுத்தவல்லது என்கிற இந்த அடிப்படைகளைப் புரிந்து நினைவில் இருத்திக் கொண்டு மேலே செல்வோம்.
- இராசேந்திர சோழன்
- விவரங்கள்
- இராசேந்திர சோழன்
- பிரிவு: தொழில்நுட்பம்
அணுவின் உட்கருவைச் சுற்றி எலக்ட்ரான் துகள்கள் பல்வேறு ஆற்றல் மட்டங்களில் சுற்றி வருகின்றன என்று பார்த்தோமில்லையா. இவ்வாற்றல் மட்டங்களை விஞ்ஞானிகள் K, L, M, N, O, P என வரையறுத்திருக்கிறார்கள்.
இதில் அணுக்கருவைச் சுற்றியுள்ள முதல் வட்டம் K, அதற்கு அடுத்த வட்டம் L, இப்படியே அடுத்தடுத்த வட்டங்களுக்குப் பெயர்.
சரி. ஒரு அணுவின் உட்கருவில் உள்ள புரோட்டான்களின் எண்ணிக்கையளவு எலக்ட்ரான்கள் அணுக் கருவைச் சுற்றி இயங்கி வருகின்றன என்று பார்த்தோமில்லையா... இவை தாறுமாறாக அது பாட்டுக்குத் தான்தோன்றித்தனமாக இயங்கிக் கொண்டிருக்கவில்லை. மாறாக, அவற்றின் இயக்கங்கள் ஒரு சீரொழுங்கான கணித வரையறைக்குட்பட்டே இருக்கின்றன.
அதாவது எந்த ஒரு அணுவிலும் அணுக்கருவைச் சுற்றியுள்ள முதல் வட்டத்தில் 2 எலக்ட்ரான்கள் இருக்கும்; அல்லது இருக்கவேண்டும்; இரண்டாவது வட்டத்தில் 8; மூன்றாவது வட்டத்தில் 18 என ஒரு சீரொழுங்கோடே இயங்கி வருகின்றது.
இந்தச் சீரொழுங்கை விளக்கும் சூத்திரத்தை 2n2 என்கிறார்கள். இதில் n என்பது ஆற்றல் மட்டத்தின் வரிசை எண்ணைக் குறிக்கும். இதன்படி ஒவ்வொரு அணுவிலும் அதைச் சுற்றியுள்ள ஆற்றல் மட்டங்களில் இயங்கி வரும் எலக்ட்ரான்களின் எண்ணிக்கை கீழ்க்கண்டவாறு அமையும்.
K 2 x 12 = 2
L 2 x 22 = 8
M 2 x 32 = 18
N 2 x 42 = 32
O 2 x 52 = 50
P 2 x 62 = 72
இந்தக் கணக்கெல்லாம் நமக்கு எதற்கு என்று சிலர் நினைக்கலாம். அப்படியல்ல இதற்குக் காரணம் இருக்கிறது. காரணம், அணு என்பது பெரும்பாலும் சில தனித்து இயங்க சாத்தியமுள்ளதும் பல தனித்து இயங்கச் சாத்தியமற்றதுமாக இருவகைப்பட்டு நிலவுகிறது.
அதற்குக் காரணம், எந்த ஒரு அணுவில் அவ்வணுக் கருவைச் சுற்றியுள்ள எலக்ட்ரான்களின் எண்ணிக்கை, அதன் ஆற்றல் மட்டங்களுக்குரிய தேவையை நிறைவு செய்கிறதோ அந்த அணு மட்டுமே நிலைப்புத் தன்மை கொண்ட அணுவாக இருக்கமுடியும். பெரும்பாலும் அப்படிப்பட்ட அணு மட்டுமே தனித்து இயங்க சாத்தியமுள்ளதாக இருக்கும், ஓரணு மூலக்கூறுள்ள அணுக்கள் இப்படித் தனித்து இயங்கவல்லவை என்று சொல்லப்படுகிறது.
அப்படி அந்த எண்ணிக்கைத் தேவையை நிறைவு செய்யாத அணுக்கள் எல்லாம் நிலைப்புத் தன்மையற்ற அணுக்கள் எனப்படுகின்றன. இந்த அணு தனித்து இயங்க முடியாது. இது ஏதாவது ஒரு குறிப்பிட்ட தனிமத்தின் அணு தான் என்றாலும், அதில் அந்த அணு ஒரு தனித்த அணுவாக இயங்க முடியாமல் இரண்டு அல்லது இரண்டுக்கு மேற்பட்ட ஒரே வித அணுக்கள் ஒன்று சேர்ந்தே அத்தனிமத்தை உருவாக்கியிருக்கும், உருவாக்கவும் முடியும்.
காட்டாக, ஆக்சிஜனில் உள்ள எலக்ட்ரான்கள் 8. இதில் முதல் வட்டத்தில் இரண்டு போக இரண்டாவது வட்டத்துக்கு 6தான் வரும் இல்லையா..? ஆனால் நியாயப்படி 8 எலக்ட்ரான் இருந்தால்தான் நிலைப்புத் தன்மை பெற முடியும். ஆகவே ஆக்சிஜன் அணு என்ன செய்கிறது? இன்னொரு ஆக்சிஜன் அணுவுடன் சேருகிறது. அந்த இன்னொரு ஆக்சிஜன் அணுவும் இரண்டாவது வட்டத்தில் 6 எலக்ட்ரான்களுடன் அலைகிறது இல்லையா..? ஆகவே இந்த இரண்டும் ஒன்று சேர்ந்து இரண்டும் சேர்ந்த நெருக்கத்தில் ஒன்றோடொன்று பிணைந்து, ஒன்றின் எலக்ட்ரான்களை மற்றொன்றுக்குப் பரஸ்பரம் தந்து, இரண்டாவது ஆற்றல் மட்டத்தின் எண்ணிக்கைத் தேவையைப் பூர்த்தி செய்து நிலைப்புத் தன்மை பெறுகிறது.
தனித்து இயங்க இயலாத இப்படிப்பட்ட நிலைப்புத் தன்மையற்ற அணுக்கள் ஒவ்வொன்றும் இவ்வாறே இரண்டு அல்லது அதற்கு மேற்பட்ட அணுக்களாகச் சேர்ந்து நிலைப்புத் தன்மை பெறுகின்றன.
இதில் ஒரு சின்ன செய்தி. இப்படி ஆற்றல் மட்டங்கள் பற்றியெல்லாம் சொல்வதால், ஒவ்வொரு அணுவிலும், அதன் ஆற்றல் மட்டங்களில் எலக்ட்ரான்கள் அடுக்கடுக்காய் வட்ட வட்டமாய் சாலை போட்ட மாதிரி அதனதன் பாதையில் சுற்றி வருகின்றன போலிருக்கிறது என்று யாரும் யந்திரகதியாய் கருதிக் கொள்ளக் கூடாது. அணுவே மிகமிக நுண்ணிய ஒரு துகள். அதிலும் மிகமிக நுண்ணிய துகள்கள் இந்த எலக்ட்ரான்கள். இப்படிப்பட்ட மிக நுண்ணிய துகள்கள், அதன் இயக்க மெல்லாம், இவ்வளவு நுட்பமானதாக அறியப்படுவதற்கு எவ்வளவு சிக்கலானதாக இருக்கும் என்பதை நாம் சற்று உணர்ந்துகொள்ள வேண்டும். ஆகவே இந்த எலக்ட்ரான்கள் பல்வேறு ஆற்றல் மட்டங்களில் சுற்றி வருகின்றன என்று சொல்லும்போது, இவை படத்தில் காட்டியுள்ளதுபோல் ஒரே நிலைத்த தடத்தில் அல்லாமல் - படம் என்பது ஒரு புரிதலுக்கானதே அன்றி அதுவே எல்லாமும் அல்ல - பல்வேறு தடத்தில் பல்வேறு அடுக்குகளைக் கொண்டதாகச் சுற்றி வருகின்றன என்பதை மட்டும் புரிந்து கொண்டால் போதும்.
அதேபோல, ஆற்றல் மட்டங்களின் எண்ணிக்கைத் தேவையை நிறைவு செய்வது என்கிற கோட்பாட்டிலும், அந்த ஆற்றல் மட்டங்களின் வரிசைக்கேற்ப, இறுதி வட்டத்தில் அதற்கு உரிய எண்ணிக்கையுள்ள எலக்ட்ரான்கள் இருந்தாக வேண்டும் என்கிற அவசியமில்லை. எனவே மிகக் குறைந்த அணு எண்ணிக்கையிலிருந்து, கூடிக் கொண்டே போகும் தனிம அணு வரிசையில் அதன் இறுதி வட்டத்துக்குப் போதுமான எலக்ட்ரான்கள் கிடைக்கப்பெறாத அணு, எட்டு எலக்ட்ரான்களை மட்டுமே பெற்றும் நிலைப்புத் தன்மை பெறும். இது பிற அணுக்களோடு சேரும் செயல்பாட்டுக்கும் பொருந்தும்.
ஆகவே, எதையும் வறட்டுத்தனமாய், யந்திரத்தனமாய்ப் புரிந்து கொள்ளாமல், அணு நிலைப்புத் தன்மை பெற சில நிபந்தனைகளைப் பூர்த்தி செய்ய வேண்டியுள்ளது என்று மட்டும் புரிந்து கொண்டால் போதும்.
அடுத்து, அணு பற்றி முக்கியமாகத் தெரிந்து கொள்ள வேண்டிய ஒன்று, அணுவில் நேர்மின்னூட்டமுடைய புரோட்டான்களும், எதிர்மின்னூட்டமுடைய எலக்ட்ரான்களும் சம அளவில் இருப்பதால் அணு மின்னூட்டமற்றதாக இருக்கிறது அல்லது மின் நடுநிலைத் தன்மையுடையதாக இருக்கிறது என்பது.
எனவே, ஒரு அணு மின்னூட்டமுடையதாக மாற, அது தன்னிடமுள்ள ஒன்று அல்லது ஒன்றுக்கு மேற்பட்ட எலக்ட்ரான்களை இழக்க வேண்டியிருக்கிறது. அல்லது ஒன்று அல்லது ஒன்றுக்கு மேற்பட்ட எலக்ட்ரான்களைப் பெற வேண்டிய தாயிருக்கிறது.
இவ்வாறு எலக்ட்ரான்களை இழந்தோ அல்லது கூடுதலாய்ப் பெற்றோ மின்னூட்டமுடையதாக மாறும் அணுவை அயனிகள் என்கிறார்கள். இவ்வாறு எலக்ட்ரான்களை இழந்த அணு நேர்மின்னூட்டமுடைய அயனியாகவும், எலக்ட்ரான்களைக் கூடுதலாகப் பெற்ற அணு எதிர்மின்னூட்டமுடைய அயனியாகவும் மாறுகிறது.
உதாரணமாக ஹைட்ரஜன், சோடியம், மக்னீசிய அணுக்கள் எலக்ட்ரான்களை இழந்து நேர் மின்னூடடமுடைய அயனிகளாக மாறுகின்றன. குளோரின், ஆக்சிஜன், புரோமின் அணுக்கள் எலக்ட்ரான்களைப் பெற்று எதிர்மின்னூட்டமுடைய அயனிகளாக மாறுகின்றன.
இம்மாற்றங்களிலாகட்டும், அதாவது அணு அயனிகளாக மாறும் மாற்றத்திலாகட்டும், அல்லது அணு நிலைப்புத்தன்மை பெறும் மாற்றத்திலாகட்டும், அணுக்கருவில் எந்த மாற்றமும் நிகழ்வதில்லை. மாறாக அணுக்கருவை அசுரவேகத்தில் பல்வேறு ஆற்றல் மட்டங்களில் சுற்றிவரும் எலக்ட்ரான் துகள்கள் மட்டத்திலேயே மாற்றங்கள் நிகழ்கின்றன என்பதை மனத்தில் இருத்திக் கொள்ள வேண்டும்.
அணுவின் வேதியியல் பண்புகள்
அணு சக்தி பற்றி எதுவோ சொல்ல ஆரம்பித்து இன்னமும் அணுசக்திக்குப் போகாமல், அணுவைப் பற்றியே நிறைய சொல்லிக் கொண்டிருப்பதுபோல் தோன்றுகிறதா.... இருக்கட்டும். பரவாயில்லை.
மின்விளக்கு எப்படி எரிகிறது என்று கேட்டால் சுவிட்சு போட்டதும் எரிகிறது என்று சொல்லலாம். அல்லது மின்னோட்டம் என்றால் என்ன? அது எப்படி பெறப்படுகிறது? மின் இணைப்பு, சுவிட்ச் இவற்றின் தேவை என்ன? என்பதையெல்லாம் விளக்கியும் சொல்லலாம். அதேபோல அணுசக்தி என்றால் என்ன? என்று கேட்டால் அணுவை உடைத்துப் பெறும் சக்தி என்று சொல்லிவிடலாம். அல்லது அணுவை விளக்கி அதன் கட்டமைப்பை விளக்கி, அதன் பண்புகளை விளக்கி, அதன்மூலம் அணுசக்தி, மற்ற சக்திகளிலிருந்து எவ்வாறு மாறுபட்டது என்றும் சொல்லலாம், இல்லையா?
ஆனால், முன்னது பொதுவானது, மேலோட்டமானது, எளிமையானது. பின்னது அடிப்படையானது, தெளிவானது, ஒரு சரியான புரிதலோடு நம்மைச் சிந்திக்க வைப்பது, சிறப்பானது. ஆகவே, அணுபற்றிய அடிப்படைகளைப் புரிந்து கொள்வதுதான் அணுசக்திபற்றிய புரிதலுக்குப் பயன்படும் என்கிற அடிப்படையில் இதுபற்றி அலுப்படையாமல் சில விஷயங்களைப் பார்த்துக்கொண்டு மேலே செல்வோம்.
சரி. பேரண்டத்தில் நாம் காணும் பொருள்கள் பலதரப்பட்டதாய் இருந்தாலும் அவை எல்லாம் அடிப்படையில் நாம் ஏற்கெனவே கண்ட 92 வகைத் தனிம அணுக்களால் ஆக்கப் பட்டவை என்று பார்த்தோம் இல்லையா...
இப்போது இந்த 92 வகைத் தனிம அணுக்களும் எப்படி தமக்குள் ஒன்று சேர்ந்து பல்வேறு பொருள்களை உருவாக்குகின்றன என்று பார்ப்போம். அதாவது இவ்வகைப் பொருள்களை உருவாக்குவதில் அணு எவ்வாறு செயற்படுகிறது என்பதைப் பார்ப்போம்.
உதாரணத்துக்கு நம் எல்லோருக்கும் தெரிந்த மிக எளிமையான எடுத்துக்காட்டான தண்ணீரையே எடுத்துக் கொள்வோம்.
தண்ணீர் என்பது வேதியியல் மொழியில் என்ன? H2O இல்லையா... அதாவது ஹைட்ரஜன் அணு இரண்டும், ஆக்ஸிஜன் அணு ஒன்றும் சேர்ந்தது தண்ணீர் ஆகிறது இல்லையா... இதைத் தண்ணீரின் ஒரு மூலக்கூறு என்பார்கள்.
ஹைட்ரஜன் அணு எண் 1. அது ஒரு புரோட்டான், ஒரு எலக்ட்ரான் கொண்டது. இதில் புரோட்டான் அணுக்கருவில் இருப்பது. ஆகவே அதைவிட்டு எலக்ட்ரானை மட்டும் எடுத்துக் கொள்வோம். அப்படி எடுத்துக்கொண்டால் ஒரு ஹைட்ரஜன் அணுவில் 1 எலக்ட்ரான், இரண்டு ஹைட்ரஜன் அணுவில் 2 எலக்ட்ரான்கள் இருக்கும் இல்லையா.... சரி இருக்கட்டும்.
அப்புறம், ஆக்ஸிஜன். அதன் அணு எண் 8. ஆகவே அதில் 8 எலக்ட்ரான்கள் இருக்கும். இதில் நாம் ஏற்கெனவே பார்த்தபடி முதல் ஆற்றல் மட்டப்பாதை K வட்டத்தில் 2 போக, இரண்டாவது L வட்டத்தில் எத்தனை மிஞ்சும்? 6 தான் இல்லையா?
ஆனால் நியாயப்படி இரண்டாவது வட்டத்தில் எத்தனை எலக்ட்ரான்கள் இருக்க வேண்டும்? 8. எட்டு இருந்தால்தானே அது நிலைப்புத்தன்மை பெற முடியும். ஆகவே அது என்ன செய்கிறது? இரண்டு ஹைட்ரஜன் அணுக்களையும் ஆயுத எழுத்து போலத் தன் இரு பக்கமும் சேர்த்துக்கொண்டு, அதிலுள்ள இரண்டு எலக்ட்ரான்களையும் எடுத்துக்கொண்டு, தன் இரண்டாவது ஆற்றல் மட்டப் பாதையைப் பூர்த்தி செய்து, நிலைப்புத்தன்மை பெற்றுவிடுகிறது. அதே சமயம் அது வேறு ஒரு பொருளின் மூலக்கூறாகவும் மாறிவிடுகிறது. தனித்து இயங்கும் சாத்தியமுள்ளதாகவும் ஆகிறது.
சரி. இன்னொரு உதாரணம் பார்ப்போம். நாம் உணவுக்குப் பயன்படுத்துகிற சாதாரண உப்பை எடுத்துக் கொள்வோம். இந்த உப்புக்கு வேதியியல் பெயர் என்ன? சோடியம் குளோரைடு. அதாவது சோடியத்தின் ஒரு அணுவும், குளோரினின் ஓர்அணுவும் சேர்ந்தது சோடியம் குளோரைடின் மூலக்கூறு.
இதில் சோடியத்தில் உள்ள எலக்ட்ரான்கள் 11. இதில் முதல் வட்டம் 2 இரண்டாவது வட்டம் 8 போக ஒன்று எஞ்சி நிற்கிறது. அதாவது ஒன்று அதிகமாக இருக்கிறது இல்லையா... இருக்கட்டும்.
அப்புறம் குளோரின். இதில் உள்ள எலக்ட்ரான்கள் 17. இதில் முதல் வட்டம் 2 இரண்டாவது வட்டம் 8 போக மீதி எத்தனை? 7. ஆனால் இறுதி வட்டத்தைப் பூர்த்தி செய்ய குறைந்தபட்சம் 8 எலக்ட்ரான்களாவது இருக்க வேண்டும் என்று பார்த்தோமில்லையா, அந்தக் குறைந்தபட்சத்துக்கு இன்னும் எத்தனை குறைகிறது? ஒன்று.
சோடியத்தில் அதிகமாக உள்ளது ஒன்று. குளோரைடில் குறைவுபடுவது ஒன்று.
எனவே, ஒரு எலக்ட்ரான் அதிகமாக உள்ள சோடியமும், ஒரு எலக்ட்ரான் குறைவுபடுகிற குளோரினும் ஒன்று சேர்ந்து ஒரு மூலக்கூறாகி, இரண்டும் தன் ஆற்றல் மட்டப் பாதையை நிறைவு செய்து நிலைப்புத் தன்மை பெற்றுவிடுகிறது.
நாம் எந்த ஒரு மூலக்கூறை எடுத்துக் கொண்டு பார்த்தாலும், அதில் அடங்கியுள்ள இரண்டு அல்லது அதற்கு மேற்பட்ட அணுக்கள் தன்னிடம் எஞ்சியுள்ள எலக்ட்ரான் துகள்களை அடுத்த அணுவுக்குத் தந்தோ, அல்லது தன்னிடம் குறைவுபடுகிற எலக்ட்ரான் துகள்களை அடுத்த அணுவிடமிருந்து பெற்றோ, எப்படியோ ஒன்று சேர்ந்து, ஒன்றோடொன்று பல்வேறு வடிவங்களில் நெருங்கிப் பிணைந்தும், குறுகியும் மூலக்கூறுகளை உருவாக்கி நிலைப்புத்தன்மை பெறுகின்றன. அதன்மூலம் கணக்கற்ற பொருள்களையும் உருவாக்குகின்றன.
பொதுவில் இச்செயல்பாட்டில் இப்படிப்பட்ட இணைவு இரு வகைப்பட்டு நிகழ்வதாக விளக்கப்பெறுகிறது.ஒன்று Covalant Bonds எனப்படும் சக பிணைப்பு. இது எலக்ட்ரான்களை ஏற்றுக் கொள்வதன் மூலம் நிகழ்கிற பிணைப்பு .மற்றொன்று Ionic Bonds எனப்படும் அயனிப் பிணைப்பு. இது எலக்ட்ரான்களை இழப்பதன் மூலம் நிகழ்கிற பிணைப்பு. உலோக அணுக்கள் எலக்ட்ரானை இழக்கும், அலோக அணுக்கள் எலக்ட்ரானை ஏற்கும் என்று சொல்லப்படுகிறது. சோடியம் ஒரு உலோகம் எனவே அது எலக்ட்ரானை இழக்கிறது. அதாவது ஒரு எலக்ட்ரானை குளோரினுக்குத் தந்து சோடியம் குளோரைடு மூலக்கூறுவை உருவாக்குகிறது
எல்லா அணுக்களும் இந்த விதிமுறைகளுக்கும், கணித வியலுக்கும் உட்பட்டே இயங்குகின்றன. பல்வேறு மூலக் கூறுகளை உருவாக்குகின்றன.
இயற்கை இம்மாதிரி கணிதவியலுக்கு உட்பட்டு இயங்குவது விசித்திரமாக இருக்கிறது இல்லையா...? இருக்கட்டும். இயற்கையின் இயக்கம் எல்லாமே கணிதவியலுக்கு உட்பட்டதுதான். அப்படி உட்படாத இயற்கை இயக்கம் என்று எதுவும் இல்லை.
சரி. இங்கேயும் நாம் முக்கியமாகக் கவனிக்க வேண்டியது - பல்வேறு அணுக்கள் ஒன்று சேர்ந்து மூலக்கூறுகளை உருவாக்கும் இந்தச் செயல்பாட்டிலும், அணுக்கருவில் எந்த மாற்றங்களும் நிகழ்வதில்லை. மாறாக அணுக்கருவைச் சுற்றிவரும் எலக்ட்ரான் துகள்கள் மட்டத்திலேயே அதாவது எலக்ட்ரான் துகள்கள் பரிமாற்றத்திலேயேதான் எல்லா மாற்றங்களும் நிகழ்ந்து விடுகின்றன என்பதுதான்.
சரி. இதுவரை பார்த்த விஷயங்களைச் சற்று சுருக்குவோம். அதாவது அணு என்பது என்ன? அணுவின் கட்டமைப்பு எப்படிப்பட்டது? அணுவில் அடங்கியுள்ள துகள்கள் யாவை? அத்துகள்கள் எப்படிப்பட்ட மின்சுமை உடையதாக இருக் கின்றன? அணுக்களின் ஐசோடோப்புகள் உருவாவதிலும், அணுக்கள் அயனியாக மாறுவதிலும், அணுக்கள் மூலக்கூறாக மாறுவதிலும், அணுக்கள் நிலைப்புத் தன்மை பெறுவதிலும் செயற்படும் நிகழ்வுகளில் அணுத்துகள்கள் எவ்வாறு இயங்குகின்றன என்று பார்த்தோம்.
இதில் எல்லாவற்றிலும் நாம் முக்கியமாக நினைவில் நிறுத்தவேண்டியது இந்த எல்லாவகைச் செயற்பாடுகளிலும், அணுவைச் சுற்றியுள்ள எலக்ட்ரான் துகள்கள் மட்டுமே மாற்றம் பெறுகின்றனவே தவிர அணுக்கருவில் எந்தவித மாற்றமும் நிகழ்வதில்லை, இன்னும் நாம் அணுக்கருவுக்குள்ளேயே நுழையவில்லை என்பதே. எனவே, நாம் அணுக் கருவுக்குள் நுழைவது பற்றி அடுத்து பார்ப்போம்.
- இராசேந்திர சோழன் (
- விவரங்கள்
- இராசேந்திர சோழன்
- பிரிவு: தொழில்நுட்பம்
பொதுவாக அணுக்கரு என்பது எப்படிப்பட்ட கட்டமைப்பைக் கொண்டதாக இருக்கிறது என்பதை ஓரளவு பார்த்தோம். ஆனால் இதுவே எல்லா அணுக்கருக்களையும் பற்றி விளக்கி விட்டதாகச் சொல்ல முடியுமா? முடியாது.
காரணம், பொதுவாக மனிதன் எப்படியிருப்பான் என்றால், அவனுக்கு இரண்டு கை, இரண்டு கால், ஒரு உடம்பு, கண், காது, மூக்கு, வாய் எல்லாம் இருக்கும் என்று சொல்லிவிட்டால் அதுவே எல்லா மனிதர்களையும் பற்றி விளக்கிவிட்டதாகச் சொல்ல முடியுமா? முடியாது.
ஏனெனில் அப்படிச் சொன்னால் அது எல்லா மனிதர்களையும் ஒரே மாதிரியாக அல்லவா... அதாவது மனிதர்களுக்குள்ளே வித்தியாசமே இல்லாமல் போனது போல் காட்டுவதாக அல்லவா ஆகிவிடும்? அப்புறம் மனிதர்களுக்குள் வேறுபாடு காண்பதுதான் எப்படி? இதே கதைதான் அணுக்கருவுக்கும். பொதுவாக ஒரு அணுக்கரு எப்படியிருக்கும் என்று சொல்லிவிட்டால் அதுவே எல்லா அணுக்கருவையும் விளக்கிவிட்டதாக ஆகாது.
அதே சமயம் எல்லா அணுக்கருவும் ஒரே மாதிரியாக இருந்து விட்டால், அதன் சேர்க்கையில் ஆக்சிஜன், ஹைட்ரஜன், கார்பன் போன்ற அலோக தனிமங்களும், இரும்பு, தங்கம், வெள்ளி போன்ற உலோக தனிமங்களும், இதுபோன்ற தனிமங்களின் சேர்க்கையில் நீர், காற்று, மண், மரம் முதலான விதம் விதமான பொருள்களும் கிடைக்காது.
ஆகவே அணுக்கருக்களில் வித்தியாசமுண்டு. இந்த வித்தியாசம் எப்படி ஏற்படுகிறது? இது ஒவ்வோர் அணுக் கருவிலும் அடங்கியுள்ள மூவகைத் துகள்களான புரோட்டான், நியூட்ரான், எலக்ட்ரான்களின் எண்ணிக்கை வேறுபாட்டால் தீர்மானிக்கப்படுகிறது.
காரணம், எல்லா அணுவின் உட்கருவிலும் ஒரே வகையான எண்ணிக்கையுள்ள புரோட்டான், நியூட்ரான்கள் அடங்கியிருக்கவில்லை. அதேபோல அணுக்கருவைச் சுற்றி வரும் எலக்ட்ரான்களின் எண்ணிக்கையும் ஒவ்வோர் அணுவுக்கும் வேறுபடுகிறது. எப்படி?
எல்லாப் பொருள்களும் துகள்களால் ஆனது என்றும், அப்படியான எந்த ஒரு பொருளை எடுத்துக் கொண்டு அதை மேலும் மேலும் சிறிய துகளாக ஆக்கிக்கொண்டே போனாலும், சாதாரண முறையில் மேலும் பகுக்க முடியாதபடி அதை எவ்வளவு சிறிய துகளாக ஆக்கினாலும் அந்தத் துகள் மாறாமல் அது எதிலிருந்து பெறப்பட்டதோ அந்தப் பொருளின் துகளாகவே இருப்பதைத் தனிமம் என்கிறார்கள் என்று ஏற்கெனவே பார்த்தோம் இல்லையா? எடுத்துக்காட்டாக, இரும்பை எவ்வளவு சிறிய துகளாக ஆக்கினாலும் அது இரும்புத் துகளாகவே இருக்கும். ஆகவே இரும்பு ஒரு தனிமம். இப்படி அலுமினியம் ஒரு தனிமம் செம்பு ஒரு தனிமம் என்று நிறைய சொல்லலாம்.
இப்படிப்பட்ட தனிமங்கள் இயற்கையில் 92 மட்டுமே இருப்பதாக விஞ்ஞானிகள் கண்டறிந்திருக்கிறார்கள். எல்லாப் பொருள்களும் அணுக்களால் ஆக்கப்பட்டவை என்கிற அடிப்படையில் இந்தத் தனிமங்களும் அணுக்களால் ஆக்கப்பட்டவையே என்பதை நாம் மறந்துவிடக்கூடாது. ஆனால் ஒரு முக்கிய வேறுபாடு இந்த 92 வகைத் தனிமங்களிலும் அடங்கியுள்ள அதன் அணுக்கள், அந்த அணுக்களில் அடங்கியுள்ள புரோட்டான், நியூட்ரான், எலக்ட்ரான் துகள்களில் வெவ்வேறு வகையான எண்ணிக்கையைக் கொண்டவையாக இருக்கின்றன. இப்படி வெவ்வேறு வகையான எண்ணிக்கையைக் கொண்டிருப்பதால் தான் இவை வெவ்வேறு வகை தனிமங்களாகவும் இருக்கின்றன.
இப்படி இவை வெவ்வேறு வகைத் தனிமங்களாக இருப்பதால்தான் இவை வெவ்வேறு விகிதத்தில் சேர்ந்து, சேர்மமாகி வெவ்வேறு விதமான பொருள்களாக உருவாகியிருக்கின்றன. இதன்படி இந்த 92 வகைத் தனிமங்களே இப்புவிக் கோளில் பேரண்டத்தில் நிலவும் எல்லா வகைப் பொருள்களுக்குமான அடிப்படையாகவும் இருக்கின்றன.
எனவே, அணுவின் வகைகளைப் புரிந்துகொள்ள நாம் இப்படிச் சொல்லாம். பேரண்டத்தில் நாம் காணும் பொருள்கள் பலதரப்பட்டதாய் இருந்தாலும் அவையெல்லாம் மேற்சொன்ன இந்த 92 வகைத் தனிமங்களால் ஆக்கப்பட்டவையே. இந்தத் தனிமங்களெல்லாம் பொதுவில் அணுக்களால் ஆக்கப்பட்டவையே என்றாலும் ஒவ்வொரு தனிமமும் அது அதற்கேயுரிய பிரத்தியேக அணுக்களால் ஆக்கப்பட்டிருக்கின்றன. அல்லது அப்படிப்பட்ட பிரத்தியேக அணுக்களைக் கொண்டிருக்கின்றன.
இவை அந்தந்த அணுக்களில் அடங்கியுள்ள புரோட்டான், நியூட்ரான், எலக்ட்ரான்களின் எண்ணிக்கையைப் பொறுத்து நிர்ணயிக்கப்படுகின்றன. அதாவது இந்த எண்ணிக்கையின் அளவைப் பொறுத்து அத்தனிமத்தின் தன்மை தீர்மானிக்கப்படுகிறது. இத்தனிமங்கள் பல்வேறு அளவுகளிலும் விகிதங்களிலும் ஒன்று சேர்ந்தும் கலந்துமே நாம் இப்பிரபஞ்சத்தில் காணும் கோடிக்கணக்கான பொருள்களாக உருப்பெறுகின்றன.
இப்படிப் பல்வேறு பொருள்களிலிருந்து அணுவுக்கு, அணுவிலிருந்து பல்வேறு பொருள்களுக்கு உள்ள பரஸ்பரத் தொடர்புகளை நாம் புரிந்து கொண்டால்தான் அணுவின் வகைகளையும் நாம் புரிந்து கொள்ள முடியும். இந்தப் பரஸ்பரத் தொடர்பு பற்றிய புரிதலில் மேற்சொன்ன 92 வகைத் தனிமங்களைத் தவிர விஞ்ஞானிகள் செயற்கையாக 21 வகைத் தனிமங்களையும் உருவாக்கியிருக்கிறார்கள். ஆக மொத்தம் 103 தனிமங்களினாலேயே இப்பேரண்டம் கட்டமைக்கப்பட்டுள்ளது என்பதையும் நாம் ஒரு தகவலாக ஒரு புறம் வாங்கி வைத்துக் கொள்வோம்.
என்றாலும், இங்கே நமக்குத் தேவையானது, எல்லாப் பொருள்களுக்கும் அடிப்படையானது, மேற்சொன்ன 92 வகைத் தனிமங்களே என்பதை மட்டும் கவனத்தில் கொண்டு அந்தந்தத் தனிமத்துக்கான அணுக்களைப் பற்றி மட்டுமே ஆராய்வோம்.
அதற்கு முன், மேற்சொன்னவற்றிலிருந்து நமக்கு ஒரு விஷயம் தெளிவாகலாம். அதாவது அணு என்று சொல்லும் போது பொதுவான அணு என்று எதுவும் கிடையாது. அணு என்பது மேற்சொன்ன 92 வகைத் தனிமங்களில் ஏதாவது ஒரு தனிமத்தின் அணுவாகவே இருக்க முடியும். இப்படி அல்லாத ஓர் அணு இயற்கையில் கிடையாது என்பதுதான் அது.
எனவே, அணு என்னும்போது அது ஆக்ஸிஜன் தனிம அணு, ஹைட்ரஜன் தனிம அணு, உறீலியம் தனிம அணு, இரும்பு தனிம அணு என்று இப்படிப்பட்ட ஏதாவது ஒரு தனிமத்தின் அணுவாகத்தான் இருக்க முடியுமே தவிர, இப்படியல்லாத பொதுவான அணுவாக எதுவும் இருக்க முடியாது.
அணு எண்ணும் நிறை எண்ணும்
இதுவரை 92 வகைத் தனிமங்கள், 92 வகைத் தனிமங்களுக்குமான 92 வகை அணுக்கள், இந்த அணுக்களின் வேறுபாடு, இதில் அடங்கியுள்ள புரோட்டான், நியூட்ரான், எலக்ட்ரான் துகள்களின் வேறுபாட்டால் நிர்ணயிக்கப்படுகிறது என்று பார்த்தோம். இல்லையா....
சரி. இப்போது மாதிரிக்குச் சில முக்கிய தனிம அணுக்களையும், அதில் அடங்கியுள்ள புரோட்டான், நியூட்ரான், எலக்ட்ரான் துகள்களின் எண்ணிக்கையையும் பார்ப்போம்.
|
தனிம அணு |
புரோட்டான் |
எலக்ட்ரான் |
நியூட்ரான் |
|
ஹைட்ரஜன் |
1 |
1 |
- |
|
ஹீலியம் |
2 |
2 |
2 |
|
கார்பன் |
6 |
6 |
6 |
|
ஆக்சிஜன் |
8 |
8 |
8 |
|
சோடியம் |
11 |
11 |
12 |
|
கந்தகம் |
16 |
16 |
16.1 |
|
இரும்பு |
26 |
26 |
29.1 |
|
தாமிரம் |
29 |
29 |
34.5 |
|
வெள்ளி |
47 |
47 |
60.9 |
|
தங்கம் |
79 |
79 |
118 |
|
பாதரசம் |
80 |
80 |
120.6 |
|
யுரேனியம் |
92 |
92 |
146 |
இந்த அட்டவணையை மேலோட்டமாகப் பார்க்கும் போதே நமக்கு ஒன்று புரிய வருகிறது இல்லையா...?
அதாவது எந்த ஒரு தனிமத்தின் அணுவிலும் அவ்வணுவின் கருவில் உள்ள நேர்மின்னூட்டமுடைய புரோட்டான் துகள்களின் எண்ணிக்கையும், கருவைச் சுற்றி அசுர வேகத்தில் இயங்கும் எதிர்மின்னூட்டமுடைய எலக்ட்ரான் துகள்களின் எண்ணிக்கையும் சமம்.
அதோடு, இவற்றின் எண்ணிக்கையைப் பொறுத்தே ஒரு தனிமத்தின் தன்மை அதாவது அது எவ்வகைத் தனிமம் என்பது தீர்மானிக்கப்படுகிறது. அல்லது அது எந்தத் தனி மத்தின் அணு என்பது அறியப்படுகிறது.
காட்டாக ஒரு அணுவில் 79 புரோட்டான்களும், 79 எலக்ட்ரான்களும் 118 நியூட்ரான்களும் இருந்தால் அது தங்க தனிமத்தின் அணு அல்லது இந்த எண்ணிக்கையுள்ள துகள்களின் சேர்க்கை தங்கம் தனிமமாகவே இருக்குமே தவிர அது வேறு எதுவாகவும் இருக்காது. இருக்கவும் முடியாது.
இதுவே மேற்சொன்ன புரோட்டான் எலக்ட்ரான் துகள்களின் எண்ணிக்கை ஒவ்வொன்று கூடுதலாகி 80 புரோட்டான்களும், 80 எலக்ட்ரான்களும் இருந்து 21 நியூட்ரான்களும் இருப்பதானால் அது பாதரசத் தனிமத்தின் அணுவாக மாறிவிடும். அதாவது இது பாதரசத் தனிமத்தின் அணு என்பதை அடையாளப்படுத்தி விடும்.
எனவேதான், ஒவ்வோர் அணுவும் அது எந்தத் தனிமத்தின் அணு என்பதைக் குறிப்பிட அத்தனிமத்தின் பெயரைக் கொண்டு குறிப்பிடுவதோடு அத்தனிமஅணுவில் அடங்கியுள்ள துகள்களின் எண்ணிக்கையையும் சேர்த்தே குறிப்பிடுகிறார்கள். நடைமுறைப் பயன்பாட்டு வசதிக்காக நபர்களின் எண்ணிக்கைக் கணக்கு எடுக்கும்போது பெயர்களுக்குப் பதில் எண் குறிப்பிட்டு அழைக்கவில்லையா... அதைப்போல அத்தனிமக் குறியீட்டின் இடது கீழ்ப்பக்கம் இந்த எண்ணைக் குறிப்பிடுகிறார்கள். இப்படிக் குறிப்பிடும் அந்த எண்ணையே ஓர் அணுவின், அணு எண் என்கிறார்கள்.
ஆகவே, ஓர் அணுவில் உள்ள புரோட்டான்கள் அல்லது எலக்ட்ரான்களின் எண்ணிக்கையை வைத்தே அந்த அணுவுக்குரிய எண் அதாவது அதன் அணு எண் தீர்மானிக்கப்படுகிறது என்பது தெளிவு. அதோடு, அந்த எண்ணை வைத்தே அது எந்தத் தனிமத்தின் அணு எனவும் அறியப்படுகிறது.
காட்டாக, நைட்ரஜன் தனிமத்தின் உட்க்கருவில் 7 புரோட்டான்களும், 7 எலக்ட்ரான்களும் இருக்கின்றன. எனவே, நைட்ரஜன் தனிமத்துக்ககான குறியீடு NI 7N என்கிறார்கள். அதேபோல மக்னீசியம் அணுக்கருவில் 12 புரோட்டான்களும், 12 எலக்ட்ரான் களும் இருக்கின்றன. எனவே, மக்னீசியம் தனிமத்துக்கான குறியீடு Mg I 12Mg என்கிறார்கள். தனிம வரிசை அட்டவணையில் உள்ள 92 வகைத் தனிமங்களும் அதன் அணு எண்ணைப் பொறுத்தவரை இவ்வாறே குறிப்பிடப்படுகின்றன.
இதில் இன்னொரு விஷயம். அணுவே மிக மிக இலேசான ஒரு துகள் என்று பார்த்தோமில்லையா.... அப்படி என்றால் அந்த அணுவுக்குள்ளும் அடங்கியுள்ள துகள்கள் எவ்வளவு நுண்ணியதாய் இருக்கும் என்று கற்பனை செய்து பாருங்கள். என்றாலும் இவ்வளவு நுண்ணிய மிக மிக இலேசான துகள்களின் நிறையையும் விஞ்ஞானிகள் கணக்கிட்டிருக்கிறார்கள்.
அதன்படி ஓர் எலக்ட்ரான் துகளின் நிறை 9.11x 10-28 கிராம் என்கிறார்கள். அதாவது 9.11ஐப் போட்டு அதை ஒன்றின் பக்கத்தில் 28 சைபர் சேர்ந்த எண்ணால் வகுத்தால் என்ன ஈவு கிடைக்குமோ அத்தனை கிராம். ஓர் எலக்ட்ரான் துகளின் நிறை. இந்த எலக்ட்ரானின் நிறையைப்போல் 1,836 மடங்கு அதிகமுடையதாம் அணுக்கருவில் உள்ள புரோட்டானின் நிறை.
ஆகவே, எந்த ஓர் அணுவிலும் புரோட்டான்கள், எலக்ட்ரான்களின் எண்ணிக்கை சமமாக இருந்தபோதிலும் அணுக்கருவில் உள்ளதும், நிறை அதிகமாயுள்ளதுமான இந்தப் புரோட்டான்களின் எண்ணிக்கையை வைத்தே அதன் அணு எண்ணைக் குறிப்பிடுவது வழக்கமாக இருந்து வருகிறது.
எனவே தான் 8O என்று குறிப்பது ஆக்சிஜன் அணுக் கருவில் 8 எலக்ட்ரான்கள் உள்ளன என்பதைக் காட்டிலும் 8 புரோட்டான்கள் உள்ளன என்பதையே அர்த்தப்படுகிறது. காரணம் அதுவே நிறை அதிகமுடையது என்பது ஒன்று. அடுத்தது, இப்படி நிறை அதிகமுடைய அத்துகள்கள் அணுவின் கருவில் அடங்கி, அணுவின் பெரும் பகுதி நிறையைத் தீர்மானிப்பதில் கணிசமான பங்காற்று கின்றன என்பது மற்றொன்று.
சரி, இதுவரை புரோட்டான்கள், எலக்ட்ரான்கள் பற்றி ஒவ்வோர் அணுவிலும் அவை சம எண்ணிக்கையில் இருப்பதையும், அவையே அணு எண்ணைத் தீர்மானிக்கின்றன என்பதையும் பார்த்தோம். சரி ஆனால் இந்த நியூட்ரான்கள் பற்றி இன்னும் ஒன்றுமே பார்க்கவில்லையே.... அணுக்கருவில் அதன் இடம்தான் என்ன? அதன் செயல்பாடுதான் என்ன? அணுக் கருவில் அந்தத் துகள்களுக்கு ஏதும் பங்கே இல்லையா....? எனக் கேள்விகள் எழலாம். நியாயம். அணுக்கருவில் நியூட்ரான் துகள்களுக்கு நிச்சயமாகப் பெரும் பங்கு உண்டு. காரணம், புரோட்டான் துகள்கள் ஒரு அணுவின் அணு எண்ணைக் குறிக்க, அறிய அடிப்படையாய் இருக்கிறது என்றால், இந்த நியூட்ரான் துகள்கள் அணுவின் பொருண்மை எண்ணை அதாவது நிறை எண்ணை அறிய அடிப்படையாயிருக்கின்றன. அதாவது இந்த நியூட்ரான் துகள்களின் எண்ணிக்கையை அடிப்படையாகக் கொண்டே அணுவின் பொருண்மை எண் - நிறை எண் அறியப் படுகிறது.
எப்படி? இந்த நியூட்ரான்கள், புரோட்டான்களுடன் சேர்ந்து அணுவின் உட்கருவில் இருப்பதாகப் பார்த்தோம் இல்லையா.... ஆனால் இவை புரோட்டான், எலக்ட்ரான் துகள்களைப் போல எண்ணிக்கையில் சம அளவை மட்டுமே கொண்டதாக இருப்பதில்லை. மாறாக, இது புரோட்டான், எலக்ட்ரான் துகள்களின் எண்ணிக்கையைப் பற்றிக் கவலைப்படாமல் அதற்குச் சமமாகவோ அல்லது அதைவிட எண்ணிக்கையில் சற்றுக் கூடுதலாகவோ குறைவாகவோ ஆக எப்படி வேண்டுமானாலும் இருக்கிறது.
அதோடு, இந்த நியூட்ரான்களும் எலக்ட்ரான்களின் நிறையை விடப் பல மடங்கு கூடுதலானவை. கிட்டத்தட்ட புரோட்டான்களின் நிறைக்குச் சமமானவை. நிறை என்பது அதில் அடங்கியுள்ள பருப் பொருள்களின் திண்மையை எடையைச் சார்ந்ததாகும்.
அணுவின் நியூட்ரான், புரோட்டான்களின் நிறை, அதைச் சுற்றி இயங்கும் எலக்ட்ரான்களின் நிறையை விட, 1836 மடங்கு, சுமாராகக் கூறின் 2000 மடங்கு அதிகம் என்கிறார்கள்.
ஆகவேதான், அணுவின் உட்கருவில் உள்ளதும் நிறை அதிகமுள்ளதுமான புரோட்டான்களின் எண்ணிக்கையையும், அதே அணுக்கருவில் உள்ளதும் புரோட்டான்களுக்குச் சமமான நிறை உடையதுமான நியூட்ரான் துகள்களின் எண்ணிக்கையையும் சேர்த்தே ஓர் அணுவின் நிறை அளவிடப்படுகிறது. அதாவது இந்தப் புரோட்டான், நியூட்ரான் துகள்களின் எண்ணிக்கையைச் சேர்த்தே ஓர் அணுவின் பொருண்மை எண்ணை-நிறைஎண்ணைக் கணக்கிடுகிறார்கள்.
உதாரணமாய் கீழ்க்காணும் அட்டவணையைப் பார்க்க இது புரியும்.
|
தனிம அணு |
எலக்ட். |
புரோட்+நியூட் |
நிறை எண் |
|
||||
|
|
ஹைட்ரஜன் |
1 |
1+0 |
1 |
||||
|
|
ஹீலியம் |
2 |
2+2 |
4 |
||||
|
|
கார்பன் |
6 |
6+6 |
12 |
||||
|
|
சோடியம் |
11 |
11+12 |
23 |
||||
|
|
இரும்பு |
26 |
26+30 |
56 |
||||
|
|
யுரேனியம் |
92 |
92+146 |
238 |
||||
இவ்வாறே நிறை எண் அறியப்படுகிறது. இப்படி அறியப்பட்ட நிறை எண்ணும் தனிம அணுவின் குறியீட்டோடு சேர்த்து எழுதப்படுகிறது. இது குறியீட்டின் வலது மேல் பக்கம் குறிக்கப்பபடுகிறது. இந்த நிறைஎண்ணிலிருந்து புரோட்டான்களின் எண்ணிக்கையைக் கழித்தால் அந்த அணுக் கருவில் உள்ள எலக்ட்ரான்களின் எண்ணிக்கை கிடைத்து விடும். காட்டாக இப்படி, 92 வகைத் தனிம அணுக்களுக்கும் ஒரு பட்டியல் போட்டால், அவ்வணுக்களில் புரோட்டான், எலக்ட்ரான்களின் எண்ணிக்கை சமமாக இருப்பதையும், அதில் புரோட்டான்களின் எண்ணிக்கையை வைத்து அணு எண் குறிப்பிடப்படுவதையும், புரோட்டான், நியூட்ரான்களின் எண்ணிக்கையை வைத்து நிறை எண் குறிப்பிடப்படுவதையும் அறியலாம். இதுவே ஒவ்வோர் அணுவுக்கும், அணு எண்ணும் பொருண்மை எண்ணும் கணக்கிடுவதற்கான முறையாகும்.
உதாரணமாக, ஹீலியம் தனிம அணுவில் இரண்டு புரோட்டான்களும் இரண்டு நியூட்ரான்களும் இருக்கின்றன. ஆகவே அதன் அணு எண் 2. பொருண்மை எண் 4. எனவே அது 2He4 என எழுதப்படுகிறது.
இரும்பு அணுவில் 26 புரோட்டான்களும், 30 நியூட் ரான்களும் இருக்கின்றன. அதன் அணு எண் 26. பொருண்மை எண் 56. எனவே 26Fe56 என எழுதப்படுகிறது.
அதே போல யுரேனிய அணுவில் 92 புரோட்டான்களும், 146 நியூட்ரான்களும் இருக்கின்றன. எனவே இது 92U238 என எழுதப்படுகிறது.
ஆக, இப்படி எழுதப்படுவதிலிருந்து கீழுள்ள அணு எண், அணுக் கருவிலுள்ள புரோட்டான்களின் எண்ணிக்கையைக் குறிப்பதையும், மேலுள்ள எண் நிறை எண் என்பதால் அது, அவ்வணுக் கருவிலுள்ள புரோட்டான் நியூட்ரான்களின் இவ்விரண்டின் எண்ணிக்கையையும் சேர்த்துக் குறிப்பதையும் அறியலாம்.
அதோடு, இந்தக் குறியீடுகளின் எண்ணிக்கை எலக்ட்ரான்களைப் பற்றிக் கவலைப்படாமல் அணுக்கருவில் உள்ள புரோட்டான், நியூட்ரான்களின் எண்ணிக்கையைப் பற்றி மட்டுமே கவலைப்படுகிறது என்பதை நாம் நினைவில் வைத்துக் கொள்ளவேண்டும்.
இதிலிருந்தே அணு என்பதில், அதாவது அணுவின் கட்டமைப்பில், ஆற்றல் மட்டங்களில் சுற்றிவரும் எலக்ட்ரான்களை விட புரோட்டான், நியூட்ரான் அடங்கியுள்ள அணுக் கருவுக்கே அதிக முக்கியத்துவம் தரப்படுகிறது என்பதையும் நாம் புரிந்து கொள்ளலாம்.
இங்கே இன்னொரு விஷயத்தையும் இலேசாய்த் தெரிந்து வைத்துக் கொள்வது பின்னால் உதவிகரமாக இருக்கும். அது என்ன?
அணு எண், நிறை எண் பற்றி இதுவரை பார்த்தவற்றிலிருந்து நமக்கு ஒன்று தோன்றலாம். அதாவது ஒரு குறிப்பிட்ட அணு எண் கொண்ட ஒரு அணு, ஒரு குறிப்பிட்ட நிறை எண் கொண்டதாக இருக்கும், அல்லது இருக்க வேண்டும் இல்லையா...?
ஆனால் அப்படி மட்டுமே இருப்பதில்லை. காரணம், புரோட்டான்கள், நியூட்ரான்களின் எண்ணிக்கையை வைத்துத் தானே நிறை எண் குறிப்பிடப்படுகிறது? இதில் ஒரே அளவு புரோட்டான் எண்ணிக்கையுள்ள ஒரு அணுவில் நியூட்ரான்களின் எண்ணிக்கை சற்றுக் கூடுதலாகவோ குறைவாகவோ இருக்கும். அதாவது ஒரே அணு எண் கொண்ட ஒரு அணுவின் நிறை எண் வெவ்வேறு விதமாக இருக்கும்.
இவ்வாறு ஒரே அணு எண் கொண்ட ஒரு அணு மாறுபட்ட நிறை எண் கொண்ட அணுவாக நிலவுவதை அந்த அணுவின் ‘ஐசோடோப்’ (Isotop) என்கிறார்கள்.
உதாரணமாய் ஹைட்ரஜன் அணுவை எடுத்துக் கொள்வோம். இது உட்கருவில் ஒரு புரோட்டானும், அதைச் சுற்றி ஒரு எலக்ட்ரானும் கொண்டது. நியூட்ரான் கிடையாது. ஆகவே இதன் அணு எண் 1. பொருண்மை எண் 1. இதைப் புரோட்டியம் (Protium) என்கிறார்கள்.
இன்னொரு ஹைட்ரஜன் உட்கருவில் ஒரு புரோட்டானும், ஒரு நியூட்ரானும் உள்ளது. உட்கருவைச் சுற்றி ஒரு எலக்ட் ரான் உள்ளது. ஆகவே இதன் அணு எண் 1. நிறை எண் 2. இதை ட்யூட்ரியம் (Deutrium) என்கிறார்கள்.
மற்றொரு ஹைட்ரஜன் அணுவின் உட்கருவில் ஒரு புரோட்டானும், ஒரு எலக்ட்ரானும் இரண்டு நியூட்ரானும் உள்ளது. ஆகவே இதன் அணு எண் 1, நிறை எண் 3. இதை ட்ரைடியம் (Tritium) என்கிறார்கள்.
மூன்றும் பொதுவில் ஹைட்ரஜன் அணுதான். அவற்றின் அணு எண் ஒன்றுதான்.என்றாலும் நிறை எண் வேறு. இவ் வேறுபாட்டுக்குக் காரணம் அணுக்கருவில் உள்ள நியூட்ரான்களின் எண்ணிக்கைதான். எனவே ஒரு தனிம அணுவில் நிலவும் நியூட்ரரான்களின் எண்ணிக்கையை வைத்து அவை வெவ்வேறு நிறை கொண்டதாக நிலவுவதையே அந்தத் தனிமத்தின் ஐசோடோப் என்கிறார்கள் என்பதை மட்டும் புரிந்து கொண்டு அடுத்துச் செல்வோம்.
- விவரங்கள்
- இராசேந்திர சோழன்
- பிரிவு: தொழில்நுட்பம்
(கூடங்குளம் அணு உலை எதிர்ப்புப் போராட்டத்தையொட்டி அணு உலைகளின் தேவை, தேவையின்மை குறித்து ஒரு விவாதம் கிளம்பியிருக்கிறது. அணு ஆற்றல் என்றால் என்ன, அதிலிருந்து மின்சாரம் எப்படி பெறப்படுகிறது, அதன் சாதக, பாதகம் என்ன என்பது குறித்து தெரியாமலே பலர் 'வளர்ச்சி' என்ற பெயரில் அதை ஆதரிக்கத் தொடங்கி விடுகின்றனர். இத்தகு சூழலில், எழுத்தாளர் இராசேந்திர சோழன் எழுதி, மங்கை பதிப்பக வெளியீடாக வந்த 'அணு ஆற்றலும் மானுட வாழ்க்கையும்' நூலின் பகுதிகளை வெளியிடுவது பொருத்தமாக இருக்கும் என்று கருதி, பகுதி, பகுதியாக கீற்றில் வெளியிடுகிறோம். வெளியிட இசைவு அளித்த இராசேந்திர சோழன் அவர்களுக்கு நன்றிகள்!! - கீற்று நந்தன்)
அணு ஆற்றலும் மானுட வாழ்க்கையும்
இராசேந்திர சோழன்
மங்கை பதிப்பகம்
700, எம்.ஐ.ஜி. இரண்டாவது தலைமைச் சாலை,
தமிழ்நாடு வீட்டுவசதி வாரியக் குடியிருப்பு,
வேளச்சேரி, சென்னை - 600 042.
( 044-43595301, செல்பேசி : 94448 65204)
***
முன்னுரை
மனித வாழ்க்கை வசதிகள் நாளும் பெருகிக் கொண்டிருக்கின்றன. வாழ்க்கைப் பயன்பாட்டிற்கான சாதனங்கள் நாளும் முன்னேறிக்கொண்டிருக்கின்றன. இவை அனைத்தும் பெருமளவும் மின் ஆற்றலைச் சார்ந்தே இயங்கி வருகின்றன. எனில், இம் மின்னாற்றலை உற்பத்தி செய்யும் வளவூற்றுகள் இன்னும் எத்தனை நாளைக்கு வரும் என்பது கேள்விக்குரியதாயிருக்கிறது.
இந்நிலையில் மாற்று வழிகளில் ஆற்றலைப் பெறுவதற்கான முயற்சிகளில் அறிவியலாளர்கள் இறங்க, அணுக்கரு ஆற்றல் இத்தேவைகளை நிறைவு செய்யும் என நம்பப்பட்டது.
அணுக்கரு ஆற்றலைப் பயன்படுத்துவதில் இருவகைத் தொழில் நுட்பங்கள் நிலவி வருகின்றன. ஒன்று அணுக்கருப் பிளப்பு; மற்றொன்று அணுக்கருப் பிணைப்பு. இவற்றுள் அணுக்கருப் பிளப்புத் தொழில் நுட்பமே இதுகாறும் பயன்படுத்தப் பட்டு வருகிறது.
எனில், இத்தொழில் நுட்பம் அளப்பரிய ஆற்றலை வழங்கும் அதே வேளை, மனித குலத்தையே நாசம் செய்யும் மிக அபாயகரமான கதிரியக்கத்தையும் வெளிப்படுத்துகிறது. அக்கதிரியக்கத்தைக் கட்டுப்படுத்தி, அதன் அபாயத்திலிருந்து மனித குலத்தைக் காப்பாற்றும் நம்பகமான தொழில்நுட்பம் என்பது இதுவரை கண்டறியப்படவில்லை.
எனவே, இதற்கு மாற்றாக அணுக்கருப் பிணைப்புத் தொழில் நுட்பம் பரிசீலிக்கப்பட்டு இதற்கான ஆய்வுகள் மேற்கொள்ளப்பட்டு வருகின்றன. ஆனால், அணுக்கருப் பிளப்பில் உள்ள அதே கதிரியக்க ஆபத்துகள் அனைத்தும் அணுக்கருப் பிணைப்பிலுமே இருப்பதாகவே ஆய்வுகள் வெளிப்படுத்துகின்றன.
இந்நிலையில் வளரும் இளம் தலைமுறையினர், குறிப்பாக மாணவர்கள், நாம் எப்படிப்பட்ட நவீன அறிவியல் உலகில் வாழ்ந்து கொண்டிருக்கிறோம், நம் வாழ்க்கைத் தேவைக்கான, சமூக இயக்கத்துக்கான ஆற்றல்கள் எங்கிருந்து எப்படி பெறப்படுகின்றன, எதிர்காலத்தில் இத்தேவைகளுக்கு நாம் என்ன செய்யப் போகிறோம் என்பது குறித்தும், இத்தேவைகளை நிறைவு செய்யும் என்பதாக நம்பப்படும் அணுக்கருத் தொழில் நுட்பம், அதன் சாதக பாதக அம்சங்கள் பற்றி ஓரளவேனும் அறிந்து, அதன் அபாயங்களை உணர்ந்து, இதற்கு மாற்றாக வேறு எப்படிப்பட்ட ஆற்றல்களைப் பயன்படுத்த முடியும் என்பது குறித்தும், தங்கள் சிந்தனையைச் செலுத்த வைக்கும் நோக்கில், சாதாரண கல்வியறிவு உள்ளவர்களும் புரிந்து கொள்ளும் வகையில் எளிமையான முறையில் எழுதப்பட்டதே இந்நூல்.
தமிழ்நாட்டில் எண்பதுகளின் தொடக்கத்தில் கூடங்குளம் அணுமின் நிலையம் நிறுவும் முயற்சிகள் மேற்கொள்ளப்பட்டபோது, மக்களுக்கு இது சார்ந்த விழிப்புணர்வை ஏற்படுத்தவேண்டும் என்கிற நோக்கில் இதுபற்றி விரிவாக எழுதப்பட்ட ஒரு நூல். செய்தி அச்சுத்தாளில் அப்போது மலிவுப் பதிப்பாக கொண்டுவரப்பட்டது.
இந்நூல் முக்கியமாக மூன்று பேருக்கு மிகுந்த நன்றிக் கடன்பட்டிருக்கிறது.
சென்னை மாநிலக் கல்லூரியில் இயற்பியல் பேராசிரியராகவும், குடியாத்தம் அரசு கல்லூரியில் முதல்வராகவும் பணியாற்றி ஓய்வு பெற்றவரும், தன் பணிக்காலத்தில் தமிழ்நாடு அரசு கல்லூரி ஆசிரியர் சங்கத்தின் தலைவர், பொதுச் செயலாளர், சென்னைப் பல்கலைக் கழக ஆட்சிமன்றக் குழு உறுப்பினர் எனப் பல்வேறு பொறுப்புகளை வகித்தவரும் தற்போதும் கல்வியியல். மனித உரிமைத் தளங்களில் தொடர்ந்து பணியாற்றி வருபவருமான அன்புத் தோழர் முனைவர் சிவக்குமார்,
அம்பத்தூர் மகளிர் மேநிலைப் பள்ளி இயற்பியல் ஆசிரியரும், சிறந்த மனிதநேயப் பற்றாளருமான திரு. அழகர்சாமி,
சென்னை மாநிலக் கல்லூரியில் தற்போது இயற்பியல் இணைப் பேராசிரியராகப் பணியாற்றி வருபவரும், 2008ஆம் ஆண்டு 10ஆம் வகுப்பு இயற்பியல் பாடநூல் தயாரிப்புக் குழுத் தலைவராகப் பொறுப்பேற்று செயல்பட்டவரும், மக்கள் தொலைக்காட்சி மற்றும் பிற ஊடகங்களில் எளிமையான முறையில் அறிவியல் நிகழ்ச்சிகள் நடத்தி வருபவருமான திரு. சுப்பையா பாண்டி,
ஆகிய மூவரும் நூலை வரிக்கு வரி படித்து தேவையான ஆலோசனைகள், திருத்தங்கள் தந்து நூல் பொருள் பிழை, கருத்துப் பிழையின்றி செம்மையாக்கம் பெற பெரிதும் உதவியிருக்கிறார்கள். இவர்கள் முன்வைத்த கருத்துகள். ஆலோசனைகள் அனைத்தையும் நூலில் கொண்டுவர என்னால் இயலாது போனாலும் முடிந்த மட்டும் அவற்றை நிறைவேற்றி இருக்கிறேன்.
எனவே,இந்நூல் அறிவியல்சார் தெளிவோடும் புரிதலோடும் வெளி வந்திருப்பதாயின் இத்தெளிவுகளுக்கான பெருமைகள் அனைத்தும் அம் மூவரையுமே சாரும். இதையும் மீறி ஏதும் பிழைகள் தென்படுமாயின் அதற்கு முழுமையும் நானே பொறுப்பு.
நூல் மீதான அக்கறை காரணமாக, நூல் பணியனைத்தும் முடித்து அச்சுக்குத் தருவதற்கு முன் ஒருமுறை கொண்டு வாருங்கள், இறுதிப் பிழைத் திருத்தம் பார்த்து விடலாம் என தோழர் முனைவர் சிவகுமார் கருத்து தெரிவித்திருந்தார். நூலை அவசரமாக அச்சுக்குத் தர வேண்டிய நிர்ப்பந்தமான சூழலில் அதை என்னால் நிறைவேற்ற இயலாது போய்விட்டது. அது மட்டும் மனசுக்கு குறையாக இருக்கிறது. அந்த ஒரு குறையைத் தவிர மற்றபடி நூல் நிறைவாக வந்திருப்பதாகவே எனக்குப் படுகிறது. அப்படி ஏதும் பிழைகள் தென்படுமாயின் அதை அடுத்தடுத்த பதிப்புகளில் சரி செய்து கொள்ளலாம் என்கிற தெம்பிருக்கிறது. இந்த மட்டில் நூல் அதன் நோக்கில் எந்த அளவுக்கு வெற்றி பெற்றுள்ளது என்பது நூலைப் படித்து வாசகர்கள் தெரிவிக்கும் கருத்தைப் பொறுத்தது.
படித்து கருத்து தெரிவியுங்கள்.
பார்ப்போம்.
- தோழமையுடன்
இராசேந்திர சோழன்
***
ஆற்றலின் தேவை
மனித இயக்கத்திற்கு எவ்வாறு ஆற்றல் தேவைப் படுகிறதோ, அதாவது நிற்க, நடக்க, ஓட, உட்கார, பணியாற்ற, மற்றும் பிற உடலுழைப்புகளுக்கு எவ்வாறு ஆற்றல் தேவைப்படுகிறதோ, அவ்வாறே சமூக இயக்கத்திற்கும் அளப்பரிய ஆற்றல் தேவைப் படுகிறது.
 காடுகளிலும், குகைகளிலும் வாழ்ந்த மனிதன், சமூக வளர்ச்சிப் போக்கில் இன்று நவீன வாழ்க்கை முறைக்கு உள்ளாக்கப்பட்டு அதி நவீன வசதிகளுடன் வாழ்ந்து வருகிறான். உரலில் நெல் குத்தி, யந்திரத்தில் மாவு அரைத்து, அம்மிக்கல்லில் மசாலா அரைத்து சமைத்த காலம் போய், இன்று ஆலைகளில் அரிசியாக்கி, கிரைண்டரில் மாவு அரைத்து, குக்கரில் சமைத்து, மிக்சியில் மசாலா, சட்னி அரைத்து வாழ்கிற நிலைக்குத் தள்ளப்பட்டிருக்கிறான்.
காடுகளிலும், குகைகளிலும் வாழ்ந்த மனிதன், சமூக வளர்ச்சிப் போக்கில் இன்று நவீன வாழ்க்கை முறைக்கு உள்ளாக்கப்பட்டு அதி நவீன வசதிகளுடன் வாழ்ந்து வருகிறான். உரலில் நெல் குத்தி, யந்திரத்தில் மாவு அரைத்து, அம்மிக்கல்லில் மசாலா அரைத்து சமைத்த காலம் போய், இன்று ஆலைகளில் அரிசியாக்கி, கிரைண்டரில் மாவு அரைத்து, குக்கரில் சமைத்து, மிக்சியில் மசாலா, சட்னி அரைத்து வாழ்கிற நிலைக்குத் தள்ளப்பட்டிருக்கிறான்.
இன்று ஒரு சாதாரண குடும்பமானாலும் மின் விளக்கு, மின் விசிறி, மிக்சி, கிரைண்டர், தொலைக்காட்சிப் பெட்டி முதலிய சில அடிப்படை வசதிகளுடன், சற்று மேம்பட்ட குடும்பங்களானால் இவற்றுடன் குளிர்சாதனப் பெட்டி, சலவை யந்திரம், குளிர்சாதன அறை, கணினி ஆகியவற்றுடனும் வாழ்வது என்பது இயல்பாகிப் போயுள்ளது.
வீடுகளில் இயங்கும் இப்படிப்பட்ட பொருள்கள் ஒருபுறம் இருக்க, மனிதன் புழங்கும் வெளி இடங்களில் போக்குவரத்து சாதனங்களுக்கு, அலுவலகங்கள், தொழிற்சாலைகளின் இயக்கத்துக்கு, இன்னமும் மனிதனுக்குத் தேவைப்படும் பல் வேறு பொருள்களின் உற்பத்திக்கு, அனைத்திற்கும் ஏராளமான ஆற்றல் தேவைப்படுகிறது.
இந்த ஆற்றல் பலவகைப்பட்டதாயிருந்தாலும், இவ் வாற்றல்கள் அனைத்தும் பெருமளவும் மின் ஆற்றலின் வழியாகவே பெறப்படுகிறது. அதாவது பெருமளவும் எந்த ஆற்றலையும் மின் ஆற்றலாக மாற்றியே நாம் பயன்படுத்தி வருகிறோம். கண நேரம் மின்சாரம் நின்றால்கூட மக்கள் எந்த அளவு தவித்துப் போகிறார்கள் என்பதை வைத்து நோக்க இதன் பயனை உணர்ந்து கொள்ளலாம்.
இப்படிப்பட்ட, சமூக வாழ்க்கைக்கு மிக இன்றியமையாத தாகிப் போன மின் ஆற்றல் ஏதோ ஆகாயத்திலிருந்து மனிதனுக்கு வழங்கப்படுவதில்லை. அல்லது இயற்கையாகவே கிடைப்பதுமில்லை. மாறாக மனிதனே இயற்கையைக் கொண்டு அதை உற்பத்தி செய்கிறான். அதாவது இயற்கையில் கிடைக்கும் பொருள்களைக் கொண்டு மனிதனே மின் ஆற்றலை உற்பத்தி செய்து கொள்கிறான்.
இப்படிப்பட்ட மின் ஆற்றல், அடிப்படையில் மூன்று வகைகளில் உற்பத்தி செய்யப்படுகிறது. முதலாவது, நீரிலிருந்து நீரின் மூலம் பெறப்படும் மின்னாற்றல், அதாவது இயற்கையான அருவிகள் மூலமோ அல்லது நீரைத் தேக்கி வைத்து வேகமாக சீறிவரச் செய்தோ அதன்மூலம் டர்பைன்களை இயக்கி அதன்வழி பெறப்படும் ஆற்றல். இரண்டாவது நிலக்கரியை எரியூட்டி வெப்பப்படுத்தி அந்த வெப்பத்தின் மூலம் பெறப்படும் ஆற்றல். மூன்றாவது அணுக்கருவைப் பிளந்து அதன் வழி வெளிப்படும் வெப்பத்தை வைத்து பெறப்படும் ஆற்றல்.
இம்மூன்று வழிகள் அன்றி சூரிய வெப்பத்திலிருந்து, காற்றாலைகளிலிருந்து, குப்பைகள் சாணங்களிலிருந்து, பிற எரி எண்ணெய்கள் வாயுக்களிலிருந்தும் மின் ஆற்றல் பெறப் படுகிறது. எனினும் இவை மிகக் குறைவான அளவே பெறப் படுகின்றன என்பதால் மிக அடிப்படையாகவும் பெருவீத அளவிலும் பெறப்படுவது மேற்குறிப்பிட்ட மூன்று வழிகளில் மட்டுமே.
இந்நிலையில் இந்த ஆற்றல், அதாவது இந்த ஆற்றலைத் தரும் இயற்கை, கனிம வளங்கள் இன்னும் எத்தனை நாளைக்கு வரும், எவ்வளவு காலம் நீடிக்கும் என்பதுதான் இன்றைய உலகில் அறிவியல் ஆய்வாளர்கள், விழிப்புணர்வு அடைந்த முன்னோடி மக்கள் முன் உள்ள முக்கிய கேள்வி.
காரணம், நாம் ஏற்கெனவே குறிப்பிட்டது போல் இந்த ஆற்றல் எதுவும் ஆகாயத்திலிருந்து கொட்டவில்லை. மாறாக மனிதன்தான் இதைத் தயாரிக்கிறான். அதுவும் வெற்றிடத்தி லிருந்தல்ல, இயற்கையிலிருந்து. எனவே, அந்த இயற்கை இன்னும் எத்தனை நாளைக்கு மனிதனுக்கு கை கொடுக்கும் என்பதுதான் சிக்கல்.
இப்போதே உலக அளவிலும், மாநிலங்கள் அளவிலும் நதி நீர்ப் பிரச்சினைகள், தகராறுகள், வழக்குகள், இத்துடன் எதிர்காலத்தில் மூன்றாம் உலகப்போர் என்று எதாவது மூண்டால் அது நீருக்கான போராகத்தான் இருக்கும் என்கின்றனர் சூழலியலாளர்கள். அந்த அளவுக்கு உலகம் கடுமையான நீர் நெருக்கடியைச் சந்திக்க இருக்கிறது. குடிக்கவே நீர் கிடைக்குமா என்கிற சந்தேகம். அப்புறம் எங்கிருந்து அதில் மின்சாரம் எடுப்பது?
அதேபோல நிலக்கரி. பூமிக்கடியில் இருக்கும் நிலக்கரியோ அல்லது எரி எண்ணெயோ இன்னும் 100 ஆண்டுகள், 200 ஆண்டுகள் வரை தாக்குப் பிடிக்குமா என்பதே சந்தேகம். அவ்வளவு வேகமாக காலியாகி வருகின்றன இவ் எரி பொருள்கள் என்கின்றனர் ஆய்வாளர்கள். இந்நிலையில் நிலைமை இப்படியே நீடித்து, பூமிக்கடியில் உள்ள எரிபொருளே முற்றாகத் தீர்ந்து போனால், அப்புறம் ஆற்றலுக்கு எங்கே போவது? மனித குல வாழ்க்கை என்னாவது? மீண்டும் கற்கால வாழ்க்கைக்கே திரும்ப வேண்டியதுதானா என்றும் கேட்கின்றனர் இவர்கள்.
ஆக, மின் ஆற்றல் தயாரிப்புக்கான இந்த இரு வள வாயில்களும் அடைபட்டு விட்டால் அடுத்து என்ன செய்வது என்கிற நிலையில்தான், இதற்கு மாற்றாக வேறு எந்த வழியுமே இல்லை என்கிற அளவில்தான், அணு ஆற்றலை முன் வைக்கின்றனர் பல அறிவியலாளர்கள்.
ஆனால், அதேவேளை, அணு ஆற்றலா, அது மிக மிக அபாயகரமானதாயிற்றே, அணு ஆற்றலோடு வெளிப்படும் கதிரியக்கம் பேராபத்தை விளைவிக்கக் கூடியதாயிற்றே, அது மனித குலத்தையே அழிவில் ஆழ்த்துவதாயிற்றே, அதைப் பற்றியா பேசுகிறீர்கள், அது வேண்டவே வேண்டாம். அதை விட்டு வேறு ஏதாவது மாற்று ஆற்றல்கள்பற்றிப் பேசுங்கள், மாற்று ஆற்றல்கள்பற்றிச் சிந்தியுங்கள் என்றும் சொல்கின்றனர் பலர்.
இந்நிலையில், இந்த இரு தரப்பினரது கருத்துகளையும் கேட்டுச் சிந்தித்து நாம் ஒரு தெளிவுக்கு வரவேண்டியது அவசியமாகிறது. அந்த வகையில் அணு என்றால் என்ன, அந்த அணுவிலிருந்து ஆற்றல் எவ்வாறு பெறப்படுகிறது. அந்த அணு ஆற்றல் பிற ஆற்றல்களிலிருந்து எவ்வாறு மாறுபட்டது. அந்த ஆற்றலின் பயன்கள் மற்றும் ஆபத்துகள் என்ன என்பது பற்றியெல்லாம் வளரும் தலைமுறையினராகிய நாம் ஓரளவேனும் தெரிந்துகொள்ள வேண்டியது மிகமிக இன்றியமையாததாகிறது. அந்த நோக்கில் அணுபற்றி முதலில் பார்ப்போம்.
அணு என்பது...
“அணுவைத் துளைத்து ஏழ்கடலைப் புகட்டி
குறுகத் தரித்த குறள்”
“அவனன்றி ஓரணுவும் அசையாது”
“அவனை அணு அணுவாகச் சித்ரவதை செய்து கொல்ல வேண்டும்”
“என்னா புத்தி சொல்லு அவன் அணுவளவும் திருந்த மாட்டான்”
என இப்படி ‘அணு’ என்கிற சொல் பண்டைய நம் தமிழ் முன்னோர்கள் காலம் முதல், தற்போதைய நடைமுறை வழக்கு வரை ஏதோ ஒரு வகையில் பயன்படுத்தப்பட்டு வருகிறது.
எனினும் இச்சொல், தற்போதைய நவீன அறிவியல் நோக்கில் அறியப்படும் ‘அணு’ என்கிற சொல்லுக்கு நிகரானதா என்றால் நிச்சயம் இல்லை. இருக்கவும் முடியாது.
காரணம். அணுபற்றித் தற்போதைய நவீன அறிவியல் உலகம் அறிந்துள்ள உண்மைகளைப் பல நூறு ஆண்டுகளுக்கு முன்னால் வாழ்ந்த நம் முன்னோர்கள் அறிந்திருப்பார்கள் என்று சொல்ல முடியாது. அறிந்திருக்கவும் வாய்ப்பில்லை.
எனவே, மேற்கூறிய ‘அணு’ என்கிற சொல், அப்போது ஏதோ ஒரு மிகச் சிறிய, மிக மிக நுண்ணிய ஒரு துகள் என்பதாகவே பொருள் கொள்ளப்பட்டிருக்க வேண்டும்.
அப்படிப்பட்ட ஒரு புரிதல், கருத்து நிலையிலிருந்து படிப்படியாக வளர்ந்து உருவாக்கம் பெற்றதே தற்போது நாம் காண்கிற ‘அணு’ என்கிற சொல். அதாவது அறிவியல் நோக்கில் தற்போது நாம் பயன்படுத்துகிற ‘அணு’ என்கிற சொல்.
இந்த அணு என்றால் என்ன? அதிலிருந்து ஆற்றல் - சக்தி எவ்வாறு பெறப்படுகிறது, என்பது பற்றியே தற்போது நாம் ஆராயப் போகிறோம்.
நாம் நமது பேரண்டத்தில் காணும் பல்வேறு பொருள்கள் பற்றிச் சற்று நினைவு கூர்வோம். அவை கல், மண், மரம், செடி கொடிகள், கால்நடைகள், மனிதன், சூரியன், சந்திரன், நட்சத்திரங்கள் எனப் பலவாக நமக்குக் காணக்கிடக்கின்றன.
இவை பல்வேறுவகையாக நமக்குக் காணப்பட்டாலும், இவையனைத்தும் நம் கண்ணுக்குத் தெரியாத மிக மிகச் சிறிய துகள்களால் ஆக்கப்பட்டுள்ளன என்பதும், இப்படிப்பட்ட துகள்களின் சேர்க்கையே பல்வேறு பொருள்களாக நம் கண்ணுக்குக் காட்சி தருகின்றன என்பதும் நமக்குத் தெரியும்.
இதைப் புரிந்துகொள்ள இப்படி யோசிக்கலாம். இப் பேரண்டத்தில் காணப்படும் எந்த ஒரு திண்மப் பொருளையும் அதை அடித்து உடைத்து நொறுக்கியோ, அரைத்தோ, மாவாக, துகள்களாக, தூசுகளாக ஆக்கிவிடலாம்.அல்லது எரித்து சாம்பலாக்கிவிடலாம், அப்படி ஆக்க முடியாத திண்மப் பொருள் என்பது உலகில் எதுவும் இல்லை என்பது தெளிவு. இத் திண்மப் பொருள்களுடன் நீர், எண்ணெய் முதலான நீர்மப் பொருள்களையும் காற்று, புகை முதலான வாயுப் பொருள்களையும் இத்துடன் சேர்த்துக் கொள்ளலாம்.
இப்படிச் சிந்திக்க, இப்பேரண்டமே ஒரே துகள் மயமாக, எல்லாம் தூசு மயமாகத் தெரிகிறது இல்லையா? இருக்கட்டும்.
சரி. இந்தத் துகள்கள், தூசுகள் என்பது என்ன? இதுவும் துகள்களின் சேர்க்கைதான். அதாவது நம் கண்ணுக்குத் தூசியாய்த் துகள்களாய்த் தெரியும் இப்பொருள்கள் நம் கண்ணுக்குத் தெரியாத கணக்கற்ற மிக மிக நுண்ணிய துகள்களின் சேர்க்கையால் ஆனது என்பதே இதன் பொருள்.
எடுத்துக்காட்டாக, கோடு என்பதே புள்ளிகளின் சேர்க்கைதான் என்பது நமக்குத் தெரியும் இல்லையா? இதன்படி கணக்கற்ற புள்ளிகளின் தொடர்ச்சியான, சீரொழுங் கோடு கூடிய சேர்க்கையே நமக்குக் கோடாய்த் தெரிகிறது என்பதுதானே கோடுகள் பற்றிய உண்மை?
சரி. புள்ளி என்பது என்ன? அதுவும் புள்ளிகளின் சேர்க்கைதான். எப்படி? அதாவது நம் கண்ணுக்குத் தெரியும் ஒரு புள்ளி, நம் கண்ணுத் தெரியாத, கணக்கற்ற பல நுண் புள்ளிகளின் சேர்க்கையால் ஆனது. நாம் நெற்றியில் வைக்கும் ஒரு பொட்டில் எத்தனை புள்ளிகள் இருக்கும் என்று சிந்தித்துப் பாருங்கள்.
இல்லாவிட்டால்... நல்ல பட்டையடிக்கும் பேனாவால் தாளில் ஒரு புள்ளி வைப்போம். பிறகு அதைவிடக் கூர்மையாக எழுதும் பேனாவால், பிறகு குண்டூசி முனையால் பக்கத்தில் ஒரு புள்ளி வைப்போம். இப்போது பட்டையடிக்கும் பேனாவால் வைத்த புள்ளியில், கூர்மையான பேனாவால் வைத்த புள்ளிகள் போல, குண்டூசி முனையால் வைத்த புள்ளிகள் போல, எத்தனை புள்ளிகள் இருக்க முடியும் என்று யோசிப்போம். இதெல்லாம் நம் கண்ணுக்குத் தெரிந்த நேரடி சோதனைகள் இல்லையா?
ஆனால் அணு என்பது நம் கண்ணால் நேரடியாகக் காணமுடியாத, கூட்டு நுண்ணோக்கியின் உதவியாலும் அறிய முடியாத மிக மிகச் சிறிய, மிக மிக நுண்மையான, மிகமிக இலேசான ஒரு துகள். ஒரு குண்டூசியின் கொண்டைப் பகுதியில் மட்டும் இலட்சக் கணக்கான அணுக்கள் உள்ளன என்று அறிவியலாளர்கள் சொல்கிறார்கள் என்றால் அணு எவ்வளவு நுண்ணியதாக இருக்கும் என்பதை நீங்களே ஓரளவு ஊகித்துக் கொள்ளலாம்.
இந்த அடிப்படைப் புரிதலில், அறிவியல் மொழியில், நம் கண்ணுக்குத் தெரியும் எந்த ஒரு பொருளையும் அடித்து, உடைத்து, நொறுக்கி, துகளாக்கி, தூசாக்கி இப்படி மேலும் மேலும் பகுத்துக்கொண்டே போனால், மேலும் பகுக்க முடியாத, அப்படிப் பகுத்தால் வேறு வேறு அணுக்களாக மாறிவிடுகின்ற கூறுள்ள ஒரு துகளையே அப்பொருளின் மூலக்கூறு என்பர்.
எடுத்துக்காட்டாக H2O என்பது தண்ணீரின் ஒரு மூலக்கூறு. அதாவது தண்ணீர் என்கிற ஒரு மூலக்கூறில் ஹைட்ரஜன் அணு இரண்டும், ஆக்சிஜன் அணு ஒன்றும் உள்ளன என்பது இதன் பொருள்.
அதாவது, இப்படிப் பகுக்கும் சாத்தியமுள்ளதையே மூலக்கூறு என்பர். எனில், இப்படிப் பகுக்க சாத்தியமில்லாமல் அல்லது எத்தனை முறை பகுத்தாலும், எவ்வளவு சிறியதாகப் பகுத்தாலும், மீண்டும் மீண்டும் அதே பொருளே வருகிற, வேறு ஒரு பொருளாய் மாறாத ஒரு துகளைத் தனிமம், தனிமத் துகள் என்பர். எடுத்துக்காட்டாக இரும்பு, தாமிரம், வெள்ளி, தங்கம், பாதரசம், யுரேனியம் முதலானவை இப்பண்புகள் கொண்டவை. இவை எவ்வளவு நுண்ணிய துகள்களாகப் பகுக்கப்பட்டாலும் அதே துகளாகவே இருக்குமே தவிர மாறாது.
எனவே இப்படிப்பட்ட தனிமங்களின் மேலும் பகுக்க முடியாத மிகமிகச் சிறிய, மிகமிக நுண்ணிய ஒரு துகளே “அணு” எனப்படுகிறது. சரி. கண்ணுக்குத் தெரியாத, கூட்டு நுண் ணோக்கியின் உதவியாலும் அறிய முடியாத இந்த அணுவை விஞ்ஞானிகள் எப்படிக் கண்டறிகிறார்கள்?
காற்று நேரடியாக நம் கண்ணுக்குத் தெரியாவிட்டாலும் அதன் அசைவை, இயக்கத்தை நாம் அறிகிறோம் இல்லையா? இப்படி நாம் அறியும் இந்தக் காற்றிலேயே ஆக்சிஜன், ஹைட்ரஜன், கார்பன்-டை-ஆக்சைடு, நீராவி எல்லாம் இருப் பதாக விஞ்ஞானிகள் கண்டறிந்து விளக்கியிருக்கிறார்கள் இல்லையா? அதே போலவே அணு ஆய்வுக்கென்று உள்ள சிறப்புக் கருவிகள், சோதனைகள்மூலம் இதைக் கண்டறி கிறார்கள்.
கண்டறிகிறார்கள் என்றால் அணு என்பது குண்டாக ஒரு பக்கம் பேசாமல் அசைவற்றுக் குந்திக்கிடப்பதையோ அல்லது இயக்கமற்று கம்மென்று ஓய்ந்து கிடப்பதையோ அல்ல. அந்தமாதிரி ஒரு நிலையில் எந்த அணுவும் இல்லை, இருக்கவும் முடியாது.
மாறாக, அணுவை அதன் இயக்கத்தில் அதன் இயல்பான போக்கில் கண்டறிகிறார்கள் விஞ்ஞானிகள். அப்படிப்பட்ட இயக்கத்திலிருக்கும் மிக மிக நுண்ணிய ஒரு துகளே நாம் அறிய இருக்கும் “அணு”.
இது மிக மிக நுண்ணிய ஒரு துகள் என்பதால் இது மிகமிகக் குறைந்த இடத்தையே அடைத்துக் கொள்ளும். இதனுடைய நிறையும் மிக மிகக் குறைவே. மிகமிகக் குறைவு என்றால் காட்டாக, ஒரு ஹைட்ரஜன் அணுவின் நிறை 1.673 ஒ 10-24 கிராம் என்கிறார்கள்.
அதாவது, 1.673ஐப் போட்டு அதை ஒன்றின் பக்கத்தில் இருபத்துனாலு சுழி சேர்ந்த ஒரு எண்ணால் வகுத்தால் என்ன ஈவு கிடைக்குமோ அந்த ஈவுதான், அவ்வளவு கிராம்தான் ஒரு ஹைட்ரஜன் அணுவின் நிறை.
இந்த மாதிரி எண்களையெல்லாம் போட்டு கணக்கிட்டுக் கொண்டிருக்க முடியாது. தலை சுத்தும். கணக்கிடுவதும் கஷ்டம் என்பதால்தான் இந்தக் கணக்கீட்டு முறையை எளிமையாக்கும் பொருட்டு அது அதற்கும் உரிய சுருக்கச் சூத்திரங்களைப் பயன்படுத்துகிறார்கள் விஞ்ஞானிகள்.
இவ்வளவு அற்பத்திலும் அற்பமான அணுவிலிருந்துதான் விஞ்ஞானிகள் அணுசக்தியை வெளிப்படுத்துகிறார்கள்... என்ன? வியப்பாக இருக்கிறதா..? அணுவே வியப்புதான். ஆனால் இது என்ன வியப்பு, அற்பத்திலும் அற்பமான இந்த அணு கொண்டிருக்கும் ஆற்றல், அதாவது சக்திதான் இவை எல்லாவற்றையும்விடப் பெரிய வியப்பு.
அந்த வியப்பு பற்றித்தான் இப்போது நாம் அறியப் போகிறோம். என்றாலும் அந்த வியப்புக்குள் புகுமுன் அணு வின் பொதுவான கட்டமைப்பு எப்படி என்பதைப் புரிந்து கொண்டு மேலே செல்வோம்.
அணுவின் கட்டமைப்பு
அணுவை மிகமிக நுண்ணிய, மிகமிக இலேசான, மிகமிக நிறை குறைந்த, மிகமிகக் குறைவான இடத்தையே அடைத்துக் கொள்ளும் ஒரு துகள் என்று பார்த்தோம் இல்லையா..?
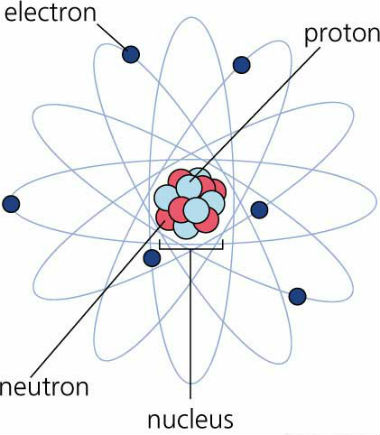 இப்போது இந்த அணுவுக்குள்ளும் அடங்கியிருக்கும் இதை விடவும் மிக மிக நுண்ணிய துகள்கள் பற்றிப் பார்க்கப் போகிறோம். எப்படி?
இப்போது இந்த அணுவுக்குள்ளும் அடங்கியிருக்கும் இதை விடவும் மிக மிக நுண்ணிய துகள்கள் பற்றிப் பார்க்கப் போகிறோம். எப்படி?
எந்த ஓர் அணுவிலும் அல்லது ஒவ்வோர் அணுவிலும், மிக மிகப் பொதுவானதும் மிக மிக அடிப்படையானதும் ஆன, முக்கியமான மூன்று வகைப்பட்ட துகள்கள் அடங்கி யிருக்கின்றன. அவையாவன :
1. எலக்ட்ரான்கள்
2. புரோட்டான்கள்
3. நியூட்ரான்கள்
இத்துகள்கள் அனைத்தும், ஓர் அணுவுக்குள் அது பாட்டுக்கு, ஒரு மூலையில் ஓய்ந்து கிடக்கவில்லை. அல்லது சகட்டு மேனிக்கு எங்குப் பார்த்தாலும் அலைந்து கொண்டிருக்க வில்லை. அல்லது ஒன்றுக்குள் ஒன்று கலந்து எல்லாம் மொத்தமாகவும் திணிந்து கிடக்கவில்லை. மாறாக, இந்த மூன்று வகைத் துகள்களும் அது அதற்கு உரிய இடத்தில், ஒப்பு நோக்கில் அது அதற்குரிய சீரொழுங்கோடு இடம் பெற்று, அது அதற்குரிய தன்மையோடு இயங்கிக் கொண்டிருக்கின்றன.
எப்படி?
எந்தவித ஓர் அணுவிலும் உட்கரு என்று ஒன்று உண்டு. இதை அணுவின் உட்கரு அல்லது அணுக்கரு என்பார்கள்.
மேற்சொன்ன மூன்று வகைத் துகள்களில், முதற் சொன்ன இரண்டு வகைத் துகள்களான புரோட்டான்களும் நியூட் ரான்களும் அணுவின் உட்கருவில் இடம் பெற்றுள்ளன.
இந்த உட்கருவைச் சுற்றி அடுக்கடுக்கான நீள்வட்டப் பாதையில் இவ்வுட்கருவை அசுர வேகத்தில் சுற்றி வரும் துகள்களாக மூன்றாவதாகச் சொன்ன எலக்ட்ரான் துகள்கள் இயங்கி வருகின்றன.
சுற்றி வரும் என்றால் அணுக்கருவுக்கு மிக நெருக்க மாகவோ அல்லது மிகப் பக்கத்திலோ அல்ல. கருவின் அளவுடன் எலக்ட்ரான் சுற்று வட்டப் பாதையை ஒப்பிடுகையில் சாதாரணமாய் ஒரு மட்டைப் பந்தாட்ட மைதானத்தின் மையப் புள்ளியில் ஒரு கோலி குண்டை வைத்து மைதானத்தின் விளிம்புச் சுற்று வட்டப் பாதையில் இன்னொரு கோலி குண்டை வேகமாகச் சுற்றிவரச் செய்தால் எந்த ஆரத்தில் சுற்றுமோ அந்த ஆரத்தில் , அல்லது விசாலமான ஒரு அறையின் மத்தியில் ஒரு ஈ உட்கார்ந்திருக்கிறது. அந்த அறையில் அந்த ஈக்கும் அறைக்கும் எவ்வளவு தூரம் இருக்குமோ அவ்வளவு தூரத்தில் இந்த எலக்ட்ரான்கள் சுற்றி வருகின்றன. சுற்றி வருகின்றன என்றால் தட்டையான ஒரு வட்டப் பாதையில் அல்ல. மாறாக மையப் பொருளைச் சுற்றி நீள்வட்டப் பாதையில் பக்க வாட்டிலும் மேல் கீழாகவும் முப்பபரிமாணம் கொண்டதாக அசுர வேகத்தில் சுற்றி வருகின்றன. இதை ரோஜா இதழ் வடிவிலான இயக்ககம் என்கின்றனர் அறிவியலாளர்கள்.
அதோடு இல்லை. இந்தத் துகள்கள் ஒவ்வொன்றும் ஒவ்வொரு வித மின்னூட்டம் கொண்டவை யாகவும் இருக்கின்றன.
அணுக்கருவிலிருக்கும் புரோட்டான்கள் நேர் மின் னூட்டம் கொண்டவை.
அணுக்கருவில் இப் புரோட்டான்களுடன் இருக்கும் நியூட்ரான்களுக்கு மின்னூட்டம் ஏதும் இல்லை. எனவே இந்த நியூட்ரான்களை மின்னூட்டமற்றவை, அல்லது மின் நடு நிலைத்தன்மையுடையவை என்கிறார்கள்.
இந்த அணுக்கருவைச் சுற்றி அசுர வேகத்தில் இயங்கி வரும் எலக்ட்ரான் துகள்கள் எதிர் மின்னூட்டம் கொண்டவையாக இருக்கின்றன.
மேற்கண்டவாறு மின்னூட்டமுயுடைய மூன்று வகையான துகள்களே எந்த ஓர் அணுக்கருவிலும் அடிப் படையில் பிரதானமாய்க் குடிகொண்டிருக்கும் முக்கிய துகள்களாகக் கருதப்படுகின்றன.
இவற்றுடன் சேர்த்து நூற்றுக்கும் மேற்பட்ட வகைப்பட்ட வெவ்வெறு துகள்களும் ஓர் அணுக்கருவுக்குள் இயங்கிக் கொண்டிருப்பதாக விஞ் ஞானிகள் கண்டறிந்திருக்கிறார்கள் என்றாலும், இப்போது நாம் அறிய இருக்கிற அணு ஆற்றல் பற்றிய புரிதலுக்கு இம் மூன்றுவகைத் துகள்கள் பற்றிய ஞானம் மட்டுமே போதும் என்பதால் இதைமட்டும் தெரிந்து இனி அடுத்தக் கட்டத்துக்குப் போவோம்.
ஆக, எந்த ஓர் அணுக்கருவிலும் மேற்சொன்ன மூன்று வகையான துகள்களும் மேற்சொன்ன கட்டமைப்பில், மேற் சொன்ன மின்னூட்டங்களோடு கூடியதாக இயங்கி வருகின்றன.
சரி. இங்கே சிலருக்குக் கேள்வி எழலாம், எழா விட்டாலும் நாமாக எழுப்பிப் பார்த்துக் கொள்ள வேண்டும். என்ன அது?
அதாவது, புரோட்டான் துகள்கள் நேர்மின்னூட்டம் உடையவை, ‘எலக்ட்ரான் துகள்கள் எதிர்மின்னூட்டம் உடையவை எனப்படுகின்றன. சரி. ஆனால், மாறுபட்ட மின்னூட்டம் ஒன்றை யொன்று ஈர்க்கும், ஒத்த மின்னூட்டம் ஒன்றையொன்று விலக்கும் என்பது பொது விதி இல்லையா...? அப்படியிருக்க புரோட்டான்களால் எலக்ட்ரான்கள் ஈர்க்கப்படாமலோ அல்லது எலக்ட்ரான்களால் புரோட்டான்கள் ஈர்க்கப்படாமலோ அது அதற்கும் உரிய இடத்தில் அது அதுவும் இயங்கி வருகிறதே. அது எப்படி என்பதுதான் அது.
இதற்குக் காரணம், அணுக்கருவுக்குள் ஓர் அடிப்படை விதி செயல் படுகிறது. உதாரணமாகப் பூமிக்கு ஈர்ப்பு விசை இருக்கிறது. அது எல்லாப் பொருள்களையும் தன்னை நோக்கி ஈர்க்கிறது. அதேபோல் பேரண்டத்தில் உள்ள எல்லாக் கோள்களும் பிற கோள்களைத் தன்னை நோக்கி ஈர்க்கின்றன. இருந்தாலும் எதுவும் ஒன்றோடொன்று போய் ஒட்டிக் கொள்ளாமலோ அல்லது மோதிக் கொள்ளாமலோ எல்லாம் அதனதன் இடத்தில் அது அதற் போய் விழுந்து பொசுங்கி விடுவதில்லை. காரணம் இந்தக் கோள்கள் எல்லாம் அது அதற்குரிய ஆற்றல் மிக்க வேகத்தில் சூரியனைச் சுற்றி வருகின்றன. இப்படிச் சுற்றி வருவதற்குத் தேவைப்படும் விசை, சூரியனின் ஈர்ப்பு விசையை எதிர்த்துச் செயல்படுகிறது. இதனாலேயே அந்தந்தக் கோள்களும் சூரியனில் போய் விழாமல் சூரியனை விட்டு விலகி, அது அதற்கும் உரிய பாதையில் சீரோடு இயங்கி வரவும் முடிகிறது.
சாதாரணமாக ஸ்ஒரு நூலில் கல்லைக் கட்டி சுழற்றுகிறோம் கல் மையத்தை நோக்கி ஈர்க்கப்படாமல் சுற்றி வருகிறது இல்லையா, சுற்றுவதை நிறுத்தினாலோ அல்லது சுற்றும் கயிறு அறுந்தாலோ என்ன ஆகும், கல் தன் சுற்று வட்டப் பாதையிலிருந்து விலகித் தளர்ந்து விடும். அல்லது சுற்றுப் பாதையிலிருந்து விலகி சுற்றும் வேகத்திற்கும் சுற்றும் திசைக்கும் ஏற்ப அத்திசை நேக்கிப் பாய்ந்து விடும். இல்லையா. இப்படி நேர்ந்து விடாமல் இருக்க, கல் அதன் பாதையில் இயங்க செயல்படும் விசையைத்தான் அதாவது, இதற்கு ஆதாரமாக இருந்து செயல்படும் விசையைத் தான் மைய நோக்கு விசை என்கின்றனர்.ஒரு குறைந்தபட்ச புரிதலுக்காக இந்த எடுத்துக் காட்டு. இது போன்று மேலும் பல எடுத்துக் காட்டுகளைக் கொண்டு நோக்க ஓரளவு இதைப் புரிந்துகொள்ளலாம்.
உதாரணமாய் நாம் வாழும் பூமி மணிக்குச் சுமார் 1,700 கி.மீ. வேகத்தில் தன்னைத் தானே சுற்றிக் கொள்கிறது. மணிக்குச் சுமார் 1லட்சம் கி.மீ. வேகத்தில் அது சூரியனைச் சுற்றிவருகிறது. இந்த வேகத்தில் அது சுற்றுவதால்தான் அது 24 மணி நேரத்தில் தன்னைத் தானேயும், 365 நாள்களில் சூரியனையும் சுற்றிவர முடிகிறது. ஆனால் பூமியில் வாழ்ந்து கொண்டிருக்கிற நமக்கு இந்த வேகம் தெரிகிறதா..? தெரியாததற்குக் காரணம் நாம் இப்புவிக்குள் பிணைந் திருப்பதுதான். இந்த வேகத்துக்குப் புவி நம்மையும் உட்படுத்திக் கொண்டு இயங்குவதுதான்.
இதேபோலவேதான் அணுக்கருவுக்குள்ளும், அதாவது கோள்களுக்கிடையேயான இயக்கத்தில் ஈர்ப்பு விசையை எதிர்த்து, அதைச் சுற்றிவரும் வேகம் செயல்படுகிறது. இதனாலேயே கோள்கள் ஒன்றையொன்று ஈர்த்து மோதிக்கொள்ளாமல் இருக்கின்றன இல்லையா? இதைப் போலவேதான் அணுக் கருவைச் சுற்றியுள்ள எலக்ட்ரான்கள், புரோட்டான்களால் ஈர்க்கப்படாமல் இருக்கின்றன. காரணம் புரோட்டான்களில் ஈர்ப்பு விசையை எதிர்த்து எலக்ட்ரான்கள் அசுர வேகத்தில் இயங்கி வருகின்றன.
இதற்கு அடிப்படையாக இயங்கும் மையநோக்கு விசை போல் மைய விலக்கு விசைஎன்றும் ஒன்று உண்டு. அறிவியல் நோக்கில் நாம் அது பற்றியும் தெரிந்து வைத்துக்கொள்வது நல்லது.
என்றாலும் இப்போதைக்கு இந்த மட்டத்துக்கு அணுவின் கட்டமைப்பைப் புரிந்துகொள்வோம். பிறகு போகப் போக பார்ப்போம்.
- மின் ஆற்றலை வழங்கும் ’செயற்கைச் சூரியன்’கள்
- லேப்டாப் பேட்டரி சக்தியை பராமரிக்க வேண்டுமா!
- அறிவியல் கருவிகளும் அவற்றின் பயன்பாடுகளும்
- உருப்பெருக்கியை உருவாக்கிய ஜோசப் ஜாக்சன் லிஸ்டர்
- வெப்பமானி எப்போது முதலில் உருவாக்கப்பட்டது?
- புதிய முறையில் மின்சார தயாரிப்பு
- மின்கலத்தில் இயங்கும் இரு சக்கர வண்டி
- டன்னல் டையோடு
- செயற்கை மூளையை உருவாக்க முடியுமா?
- ஒரு பொருளை நாம் பார்ப்பது எப்படி?
- கூடங்குளம் மின்திட்டம் - மாற்று சிந்தனை + எரிபொருள்
- மின்னணுவியல் மூக்கு
- தண்ணீருக்குள் சுவாசிக்க ஒரு திரவ நுரையீரல்
- EPR சோதனை என்பது என்ன?
- வேதியியலின் கதை – 8
- புழை இருவாயின் செயல்பாடு(Function of tunnel diode)
- அணு உலைகளுக்கு மாற்று - மூடி மறைக்கப்பட்ட உண்மைகள் - 2
- அணுஉலைகளுக்கு மாற்று - மூடி மறைக்கப்பட்ட உண்மைகள் - 1
- ஐன்ஸ்ட்டீன் கோட்பாடு ஆட்டம் காண்கிறது!
- ஒளிரும் புரதங்கள்
